Фторид молибдена(VI)
| Фторид молибдена(VI) | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Фторид молибдена(IV) |
| Традиционные названия | фтористый молибден |
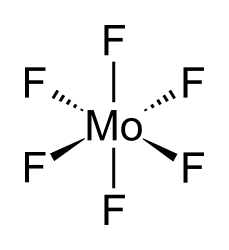
| Хим. формула | MoF6 |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 209,93 г/моль |
| Плотность | 2,543; 2,55; 2,885 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 17; 17,58 °C |
| • кипения | 33,88; 36; 38,88 °C |
| Мол. теплоёмк. | 120,5 Дж/(моль·К) |
| Энтальпия | |
| • образования | -1578 кДж/моль |
| Классификация | |
| Рег. номер CAS | 7783-77-9 |
| PubChem | 82219 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Фторид молибдена(VI) — неорганическое соединение, соль металла молибдена и плавиковой кислоты с формулой MoF6, бесцветная подвижная жидкость, реагирует с водой.
Получение
- Реакция молибдена и фтора:
- [math]\displaystyle{ \mathsf{Mo + 3F_2 \ \xrightarrow{20-50^oC}\ MoF_6 } }[/math]
- Действие фтора на гексакарбонил молибдена:
- [math]\displaystyle{ \mathsf{Mo(CO)_6 + 9F_2 \ \xrightarrow{50-70^oC}\ MoF_6 + 6CF_2O } }[/math]
- Реакция молибдена и трифторида брома:
- [math]\displaystyle{ \mathsf{Mo + 2BrF_3 \ \xrightarrow{350^oC}\ MoF_6 + Br_2 } }[/math]
Физические свойства
Фторид молибдена(VI) образует бесцветную подвижную жидкость.
При температуре ниже -9,76°С образует кристаллы ромбической сингонии, а выше этой температуры — кубической сингонии, параметры ячейки a = 0,6221 нм, Z = 2.
Растворяется в безводном фтороводороде (образует азеотропную смесь), трифториде хлора, органических растворителях.
Химические свойства
- Реагирует с влагой из воздуха:
- [math]\displaystyle{ \mathsf{2MoF_6 + 3H_2O \ \xrightarrow{}\ MoOF_4 + MoO_2F_2 + 6HF } }[/math]
- Реагирует с водой:
- [math]\displaystyle{ \mathsf{MoF_6 + 3H_2O \ \xrightarrow{}\ MoO_3\downarrow + 6HF } }[/math]
- Реагирует с разбавленными щелочами:
- [math]\displaystyle{ \mathsf{MoF_6 + 8NaOH \ \xrightarrow{}\ Na_2MoO_4 + 6NaF + 4H_2O } }[/math]
- Восстанавливается водородом или металлическим молибденом до фторида молибдена(V):
- [math]\displaystyle{ \mathsf{2MoF_6 + H_2 \ \xrightarrow{150-200^oC}\ 2MoF_5 + 2HF } }[/math]
- [math]\displaystyle{ \mathsf{5MoF_6 + Mo \ \xrightarrow{400^oC}\ 6MoF_5 } }[/math]
- С концентрированными растворами фторидов щелочных металлов образует комплексы:
- [math]\displaystyle{ \mathsf{MoF_6 + 2KF + 2H_2O \ \xrightarrow{0^oC}\ K_2[MoO_2F_4]\downarrow + 4HF } }[/math]
Применение
- Нанесение покрытия молибдена на неметаллические поверхности.
- Как компонент катализатора гидратирования нефтепродуктов.
- При разделении изотопов молибдена.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
- Неорганическая химия / под ред. Ю.Д. Третьякова. — М.: Академия, 2007. — Т. 3. — 352 с.