Фторид иридия(VI)
| Фторид иридия(VI) | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Фторид иридия(VI) |
| Традиционные названия | Фтористый иридий |
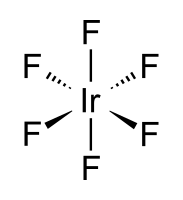
| Хим. формула | IrF6 |
| Физические свойства | |
| Состояние | жёлтые кристаллы |
| Молярная масса | 306,2 г/моль |
| Плотность | 6,0 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 44,1; 44,4 °C |
| • кипения | 53; 54 °C |
| Энтальпия | |
| • образования | -580 кДж/моль |
| Классификация | |
| Рег. номер CAS | 7783-75-7 |
| PubChem | 3014587 |
| SMILES | |
| Безопасность | |
| Токсичность | очень ядовит |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Фторид иридия(VI) — неорганическое соединение, соль металла иридия и плавиковой кислоты с формулой IrF6, жёлтые кристаллы, реагирует с водой.
Получение
- Нагревание порошкообразного иридия в атмосфере фтора:
- [math]\displaystyle{ \mathsf{Ir + 3F_2 \ \xrightarrow{250^oC}\ IrF_6 } }[/math]
Физические свойства
Фторид иридия(VI) образует жёлтые кристаллы.
Химические свойства
- Энергично реагирует с водой:[1]
- [math]\displaystyle{ \mathsf{6IrF_6 + 18H_2O \ \xrightarrow{}\ 36HF + 1.5O_2\uparrow + O_3\uparrow + 6IrO_2} }[/math]
- Реагирует с металлическим иридием:
- [math]\displaystyle{ \mathsf{2IrF_6 + Ir \ \xrightarrow{150^oC}\ 3IrF_4 } }[/math]
Примечания
- ↑ Неорганическая химия / под ред. Ю.Д. Третьякова. М., Академия, 2007. С. 146.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.