Азеотропная смесь
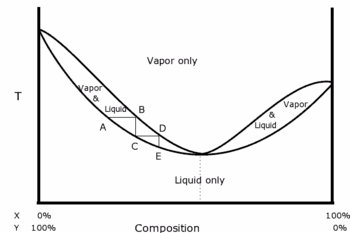
Азеотро́пная смесь — смесь двух или более жидкостей с таким составом, который (при данном конкретном давлении) не меняется при кипении, то есть составы равновесных жидкой и паровой фаз совпадают.
Смысл понятия
Точка на фазовой диаграмме, которая соответствует равенству составов жидкости и пара, называется азеотропной точкой. Температура кипения для азеотропной смеси может быть как меньше (положительные азеотропы), так и больше (отрицательные азеотропы) температуры кипения низкокипящего компонента. Термодинамика не накладывает ограничений на число азеотропных точек в системе[1]. В основном известны бинарные растворы с одной азеотропной точкой. При изменении давления изменяется не только температура кипения, но и состав азеотропной смеси, этим они отличаются от чистых жидкостей.
Показательный пример
Примером азеотропного раствора с единственной азеотропной точкой служит смесь воды и этилового спирта, содержащая 95,5 % спирта (по массе) и кипящая при атмосферном давлении при температуре 78,1°C[2][3]. Этим объясняется принятая промышленная концентрация этилового спирта 96 %: это азеотропная смесь, и дальнейшей перегонкой её при атмосферном давлении нельзя разделить на фракции, однако при пониженном давлении можно получить и большую концентрацию этанола (см. далее).
Способы разделения
Для разделения азеотропных смесей используют различные технологии:
- Химическое связывание одного из компонентов. Например, получение абсолютного спирта связыванием воды водоотнимающим веществом[K 1] (негашёной известью CaO или прокаленным сульфатом меди CuSO4[4]);
- Удаление одного из компонентов за счёт адсорбции на твёрдом пористом материале;
- Разделение на пористых мембранах;
- Первапорация на непористых мембранах;
- Перегонка при давлении, отличном от атмосферного, в частности — под вакуумом. При понижении давления изменяется азеотропный состав для данной температуры, более летучий компонент убывает из жидкой фазы. Ниже определенного давления азеотропная точка может исчезать, например, при 70 мм. рт. ст. этанол кипит при 28°С без образования азеотропа с водой.
- Перегонка с дополнительным компонентом, с созданием тройного (или более) азеотропа.
Зеотропные смеси
Смесь, в которой равенство составов равновесных жидкой и паровой фаз не выполняется ни при каком соотношении количеств компонентов, называется зеотропной. Зеотропы (называемые иногда неазеотропами), то есть раздельно кипящие системы, при заданных температуре или давлении в состоянии равновесия имеют различные составы жидкости и пара во всём интервале концентраций. Зеотропные системы, состоящие из одной жидкой фазы (растворы), называются гомозеотропами, а состоящие из двух и более жидких фаз — гетерозеотропами. Любой гомозеотропный раствор кипит при температуре ниже температуры кипения менее летучего компонента, но выше температуры кипения более летучего компонента[1].
См. также
- Эвтектика — смесь (сплав) твердых веществ, плавящаяся при одной температуре.
Комментарии
- ↑ Обычное осушающее средство — гранулированный хлорид кальция CaCl2 — в данном случае непригоден, поскольку он реагирует со спиртом с образованием соединения 3СаСl2•С2Н5ОН.
Примечания
- ↑ 1,0 1,1 Дуров, Агеев, 1987, с. 72.
- ↑ Lange’s Handbook of Chemistry, 10th ed. pp. 1496—1505
- ↑ CRC Handbook of Chemistry and Physics, 44th ed. pp 2143—2184
- ↑ Получение абсолютного спирта
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1 (Абл-Дар). — 623 с.
- Азеотропная смесь // Казахстан. Национальная энциклопедия. — Алматы: Казахская энциклопедия, 2004. — Т. I. — ISBN 9965-9389-9-7. (CC BY-SA 3.0)
- Дуров В. А., Агеев Е. П. Термодинамическая теория растворов неэлектролитов. — М.: Изд-во Моск. ун-та, 1987. — 247 с.
- Азеотропные смеси / Агеев Е. П. // Большая российская энциклопедия [Электронный ресурс]. — 2016.