Трифторид бора
| Трифторид бора | |
|---|---|
 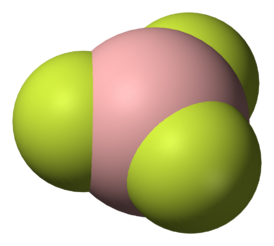 | |
| Общие | |
| Систематическое наименование |
Фторид бора(III) |
| Сокращения | Трифторобор |
| Традиционные названия | Трифторид бора; бор трёхфтористый, бора фторид, флюбор |
| Хим. формула | BF3 |
| Рац. формула | BF3 |
| Физические свойства | |
| Состояние | бесцветный ядовитый газ с резким неприятным запахом |
| Молярная масса | 67,8062 г/моль |
| Плотность | 0,00299 (+20 °C) |
| Термические свойства | |
| Температура | |
| • плавления | −126,8 °C |
| • кипения | −100,3 °C |
| Энтальпия | |
| • образования | −1137 кДж/моль |
| Структура | |
| Дипольный момент | 0 (+20 °C) |
| Классификация | |
| Рег. номер CAS | 7637-07-2 |
| RTECS | ED2275000 |
| Безопасность | |
| Предельная концентрация | 1 мг/м³[1] |
| ЛД50 | 80 мг/кг |
| Токсичность | Класс опасности (по ГОСТ 12.1.005-76): 2-й[2] |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Трифтори́д бо́ра (фторид бора(III), фторид бора(+3); флюбор, бор трёхфтористый) — бинарное неорганическое соединение бора и фтора с химической формулой BF3. Бесцветный газ с резким неприятным запахом, реагирует с водой; ядовит.
Описание
Трифторид бора BF3 при стандартных условиях представляет собой бесцветный токсичный газ с удушливым запахом, дымящий во влажном воздухе[3]. Образует аддукты со спиртами, простыми эфирами, альдегидами, кетонами, органическими основаниями, неорганическими и органическими кислотами. Трифторид бора реагирует с водой. Имеются также данные о том, что данное вещество может растворяться в ней (332,1 г в 100 г Н2О при 0 °C, 772 МПа, с частичным гидролизом), водных растворах HF, многих органических растворителях. При температуре выше +20 °C образует неустойчивые моногидрат и дигидрат[3].
Получение
- [math]\displaystyle{ \mathsf{2B + 3 F_2 \longrightarrow 2 BF_3} }[/math]
- Взаимодействие оксида бора со фтороводородом:
- [math]\displaystyle{ \mathsf{B_2O_3 + 6 HF \longrightarrow 2 BF_3 + 3 H_2O} }[/math]
- Сплавление тетрафторбората калия с борным ангидридом[4].
Химические свойства
Является сильной кислотой Льюиса. Образует комплексы с большим количеством соединений (амины, сульфиды, простые эфиры). Комплекс с диэтиловым эфиром (эфират трифторида бора, [math]\displaystyle{ BF_3 \cdot Et_2O }[/math]) — коммерчески доступный реагент.
При растворении в водной плавиковой кислоте даёт сильную тетрафторборную кислоту, являющуюся суперкислотой.
Основные сферы использования
- Трифторид бора применяют в качестве наполнителя в ионизационных камерах для детектирования нейтронов благодаря захвату нейтронов бором-10 с образованием ядер лития-7 и гелия-4, ионизирующих газ.
- Используется в качестве катализатора в органическом синтезе.
- Ограниченно использовался в упаковке пищевых продуктов (сейчас перестал использоваться из-за токсичности)[5].
Физиологическое действие

Трифторид бора - едкое, весьма токсичное вещество, обладает ярко выраженным удушающим действием. При более высоких дозах трёхфтористый бор может обладать также и общетоксическим действием.
ЛД50 для крыс составляет около 80 мг на 1 кг живого веса.
Предельно допустимая концентрация (ПДК) фторида бора(+3) в воздухе рабочей зоны производственных помещений составляет 1 мг/м³ (с обязательным контролем по фтористому водороду HF).
Класс опасности - 2 (вещества высокоопасные) по ГОСТ 12.1.005-76.
Предельно допустимые концентрации в воде
ПДК в воде составляют:
- 0,5 мг/дм3 (бор; II класс опасности);
- 1,5 мг/дм3 (фториды; II класс опасности), лимитирующий признак вредности - санитарно-токсический[6].
Примечания
- ↑ name=https://docs.cntd.ru_ГОСТ 12.1.005-76. Воздух рабочей зоны. Санитарно-гигиенические требования
- ↑ name=https://docs.cntd.ru_ГОСТ 12.1.007-76. Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ↑ 3,0 3,1 [www.xumuk.ru/encyklopedia/602.html Трифторид бора на XuMuK.Ru]
- ↑ [www.xumuk.ru/spravochnik/395.html XuMuK.Ru — сайт о химии].
- ↑ name=https://safework.ru_Boranes (недоступная ссылка)
- ↑ name=https://docs.cntd.ru_Метод (недоступная ссылка) определения бора