Фторид кислорода(II)
| Фторид кислорода(II) | |
|---|---|
  | |
| Общие | |
| Систематическое наименование |
Фторид кислорода(II) |
| Рац. формула | OF2 |
| Физические свойства | |
| Состояние | бледно-жёлтый газ |
| Молярная масса | 54 г/моль |
| Плотность | 1,59 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | -224 °C |
| • кипения | -145 °C |
| • разложения | выше 200 °C |
| Критическая точка | -58 °C, 49 атм |
| Энтальпия | |
| • образования | -25,2 кДж/моль |
| Классификация | |
| Рег. номер CAS | 7783-41-7 |
| Безопасность | |
| ЛД50 | LC50: 1-2 мг/м3*1 час (крысы, ингаляция) |
| Токсичность | Чрезвычайно ядовит, СДЯВ |
| Пиктограммы ECB |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
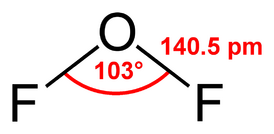
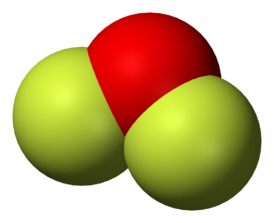
Фторид кислорода(II), дифторид кислорода, OF2. При нормальных условиях представляет собой бесцветный ядовитый газ, конденсирующийся при охлаждении в светло-жёлтую (в толстых слоях золотисто-жёлтую) жидкость. Фторид кислорода(II) имеет раздражающий запах, несколько отличающийся от запаха фтора (смесь запаха хлорной извести и озона).
Открытие
Дифторид кислорода был открыт впервые в 1929 году Полем Лебо и Августином Дамьеном, а спустя некоторое время подробно изучен Руффом и Менцелем.
Систематическое название
В литературе иногда это соединение называют оксидом фтора (F2O). Однако это неверно, так как атом фтора более электроотрицателен, чем кислород, и по правилам IUPAC это соединение должно называться именно фторидом кислорода (OF2). Хотя общая электронная пара практически не смещается от атома кислорода в сторону атома фтора.
Физические свойства
Жидкий фторид кислорода неограниченно смешивается с жидкими озоном, фтором, кислородом. Плохо растворяется в холодной воде (примерно 7:100 по объёму). При этом достаточно хорошо растворяет воздух.
Молекула обладает слабым дипольным моментом, равным 0,3 Д.
Получение
- Получение фторида кислорода(II) до сих пор проводят по так называемому «щелочному» способу пропусканием газообразного фтора в 2 % (0,5 н.) водный раствор гидроксида натрия (NaOH). Помимо фторида кислорода(II) параллельно образуются пероксид водорода и озон:
- [math]\displaystyle{ \mathsf{2F_2 + 2NaOH \rightarrow OF_2\uparrow + 2NaF + H_2O} }[/math]
- [math]\displaystyle{ \mathsf{24F_2 + 18NaOH \rightarrow 9OF_2\uparrow + 12HF + 18NaF + 3H_2O_2+ O_3\uparrow} }[/math]
- Возможно также получение фторида кислорода(II) электролизом водного раствора HF.
- При горении воды в атмосфере фтора также частично образуется дифторид кислорода и пероксид водорода. Это происходит за счёт протекания радикальных реакций:
- [math]\displaystyle{ \mathsf{F_2 + H_2O \rightarrow 2HF\uparrow + O:} }[/math] — инициация свободных радикалов с образованием бирадикала O:
- [math]\displaystyle{ \mathsf{2O: \rightarrow O_2} }[/math] — доминирующий процесс
- [math]\displaystyle{ \mathsf{O: + H_2O \rightarrow H_2O_2} }[/math]
- [math]\displaystyle{ \mathsf{O: + F_2 \rightarrow OF_2\uparrow} }[/math]
Чтобы получить чистый фторид кислорода взаимодействием воды со фтором, то нужно проводить эту реакцию при -40°C. Реакция идёт по радикально-цепному механизму:
[math]\displaystyle{ \mathsf{H_2O + 2F_2\xrightarrow{-40^oC}\ OF_2\uparrow + 2HF} }[/math]
Взаимодействие кислорода со фтором под действием ультрафиолета или электрического разряда. Кислород даже под действием ультрафиолета разлагается на свободные радикалы:
[math]\displaystyle{ \mathsf{O_2 + 2F_2 \xrightarrow{UV}\ 2OF_2\uparrow} }[/math]
Химические свойства
Дифторид кислорода — весьма энергичный окислитель, и в этом отношении напоминает по силе свободный фтор, а по механизму окисления — озон, но реакции с участием фторида кислорода(II) требуют более высокой энергии активации, так как на первой стадии происходит образование атомарного кислорода (как и у озона). Термическое разложение фторида кислорода(II) представляет собой мономолекулярную реакцию с энергией активации 41 ккал/моль и начинается только при температуре выше 200 °C.
При растворении в горячей воде подвергается гидролизу. При этом образуется фтороводород и обычный кислород. В щелочной среде разложение протекает достаточно быстро.
Смесь паров дифторида кислорода и воды взрывоопасна:
- [math]\displaystyle{ \mathsf{OF_2 + H_2O \rightarrow 2HF\uparrow + O_2\uparrow} }[/math]
Фторид кислорода(II) не действует на сухое стекло и кварц, но действует (интенсивно) на металлическую ртуть, что исключает применение ртути в приборах с фторидом кислорода(II). На смазку для газовых кранов фторид кислорода(II) действует очень медленно.
Взаимодействие с металлами
На меди, платине, золоте, серебре фторид кислорода(II) образует лишь тончайшие защитные плёнки фторидов, что позволяет использовать эти металлы в контакте с фторидом кислорода(II) при комнатной температуре. При повышении температур до 250°C происходит дальнейшее окисление металлов. Наиболее подходящими металлами для работы с дифторидом кислорода являются алюминий и магний. Нержавеющие стали, никель, монель-металл, магниевомедный сплав (92/8), латунь и медь также мало изменяются в весе при воздействии фторида кислорода(II) в течение 1-1,5 недели при 100 °C.
Применение
Благодаря высокой энергии активации разложения фторида кислорода(II), это соединение можно сравнительно безопасно смешивать с многими углеводородами, водородом, моноокисью углерода и прочими веществами, что чрезвычайно важно в практическом плане использования фторида кислорода(II) в качестве высокоэффективного окислителя ракетного топлива. Так как фторид кислорода(II) не взрывается при смешивании с горючими материалами и при нагревании (сам по себе) то его применение вполне безопасно.
Имели значительный успех опыты применения фторида кислорода(II) в газодинамических химических лазерах. Имея лучшие показатели, нежели фтор, фторид кислорода(II) способен занять достойное место в качестве компонента для боевого лазерного оружия высокой мощности[источник не указан 3728 дней].
Токсичность
Фторид кислорода(II) OF2 (дифторид кислорода) чрезвычайно токсичен (степень токсичности сопоставима с таковой фосгена COCl2), гораздо более ядовит, чем элементарный фтор, так как вызывает сильнейшее раздражение тканей организма, очень глубоко проникает и растворяется в них (глубже чем фтор), затрудняет дыхание. По токсикологии NFPA 704 ему присвоена высшая токсичность. Класс токсичности – 1.
Смертельная доза (LC50) - 1-2 мг/м3*1 час (даже меньше, чем у синильной кислоты).
Дифторид кислорода опасен для окружающей среды.
Упоминания в литературе
В фантастической новелле Роберта Л. Форварда «Камелот 30К», дифторид кислорода был использован как биохимический растворитель для живых форм, живущих в поясе Койпера Солнечной системы. Хотя при 30 К фторид кислорода будет твердым, вымышленные инопланетные организмы являются эндотермическими и благодаря радиотермическому нагреву могут использовать жидкий фторид кислорода в качестве крови.
См. также
Примечания
Литература
- С.Сарнер. Химия ракетных топлив. изд «Мир», Москва, 1969.г.
- Schmidt E. W.,Harper J. T., Handling and Use of Fluoride and Fluorine-Oxygen Mixtures in Rocket Systems, Lewis Research Center, NASA SP-3037, Cleveland, Ohio, 1967.
