Энергия активации
Для улучшения этой статьи желательно: |

Энергия активации в химии — эмпирически определяемый параметр, характеризующий показательную зависимость константы скорости реакции от температуры[1]. Выражается в джоулях на моль. Термин введён Сванте Августом Аррениусом в 1889. Типичное обозначение энергии активации: Ea.
Энергия активации в физике — минимальное количество энергии, которое должны получить электроны донорной примеси, для того чтобы попасть в зону проводимости.
В химической модели, известной как Теория активных соударений (ТАС), есть три условия, необходимых для того, чтобы произошла реакция:
- Молекулы должны столкнуться. Это важное условие, однако его не достаточно, так как при столкновении не обязательно произойдёт реакция.
- Молекулы должны обладать необходимой энергией (энергией активации). В процессе химической реакции взаимодействующие молекулы должны пройти через промежуточное состояние, которое может обладать большей энергией. То есть молекулы должны преодолеть энергетический барьер; если этого не произойдёт, реакция не начнётся.
- Молекулы должны быть правильно ориентированы относительно друг друга.
При низкой (для определённой реакции) температуре большинство молекул обладают энергией меньшей, чем энергия активации, и неспособны преодолеть энергетический барьер. Однако в веществе всегда найдутся отдельные молекулы, энергия которых значительно выше средней. Даже при низких температурах большинство реакций продолжают идти. Увеличение температуры позволяет увеличить долю молекул, обладающих достаточной энергией, чтобы преодолеть энергетический барьер. Таким образом повышается скорость реакции.
Для большинства реакций Ea = 50 — 200 кДж/моль.
Математическое описание
Уравнение Аррениуса устанавливает связь между энергией активации и скоростью протекания реакции:
- [math]\displaystyle{ E_a = -RT \ln \left( \frac{k}{A} \right) }[/math],
где k — константа скорости реакции, [math]\displaystyle{ A }[/math] — предэкспоненциальный множитель (фактор частоты) для реакции, [math]\displaystyle{ R }[/math] — универсальная газовая постоянная, [math]\displaystyle{ T }[/math] — температура в кельвинах.
С повышением температуры растёт вероятность преодоления энергетического барьера.
Для количественного описания температурных эффектов в химической кинетике для приближённых вычислений кроме уравнения Аррениуса используют правило Вант-Гоффа: повышение температуры на 10 К увеличивает для большинства реакций скорость в 2-4 раза (для биохимических реакций 7-9 раз). Математически это означает, что скорость реакции зависит от температуры степенным образом:
- [math]\displaystyle{ \mathsf{ \frac{w(T_2)}{w(T_1)} =\gamma^{\frac{T_{2}-T_{1}}{10}}} }[/math]
где [math]\displaystyle{ \gamma }[/math] — температурный коэффициент скорости (его значение лежит в интервале от 2 до 4). Правило Вант-Гоффа является весьма грубым и применимо только в очень ограниченном интервале температур: от 10 до 400 ˚С, а также при энергии активации от 60 до 120 кДж/моль. Правило Вант-Гоффа не работает с крупными молекулами.
Переходное состояние
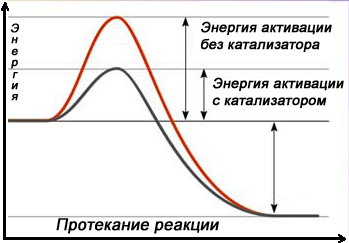
Переходное состояние — состояние системы, при котором уравновешены разрушенные и созданные связи. В переходном состоянии система находится в течение небольшого (10−15 с) времени. Энергия, которую необходимо затратить, чтобы привести систему в переходное состояние, называется энергией активации. В многоступенчатых реакциях, которые включают в себя несколько переходных состояний, энергия активации соответствует наибольшему значению энергии. После преодоления переходного состояния молекулы вновь разлетаются с разрушением старых связей и образованием новых или с преобразованием исходных связей. Оба варианта возможны, так как происходят с высвобождением энергии (это хорошо видно на рисунке, поскольку оба положения лежат энергетически ниже энергии активации). Существуют вещества, способные уменьшить энергию активации для данной реакции. Такие вещества называют катализаторами. В биологических реакциях в качестве катализаторов выступают ферменты.
Утверждение о том, что катализатор снижает энергию активации, строго говоря, не корректно, так как реакция в присутствии катализатора не идентична исходной реакции[2]. Просто это совершенно иная реакция, имеющая более низкий активационный барьер.
См. также
Примечания
- ↑ International Union of Pure and Applied Chemistry. IUPAC Gold Book - activation energy (Arrhenius activation energy) (англ.). goldbook.iupac.org. Дата обращения: 21 января 2019.
- ↑ Jan Koolman, Klaus-Heinrich Rohm, 207 Farbtafeln von Jurgen Wirth. Катализ. Taschenatlas der Biochemie, http://www.chem.msu.ru/rus/teaching/kolman/03.htm. Москва “Мир” 2000: Georg Thieme Verlag Stuttgart · New York (1998).