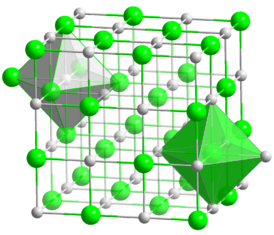
Оксид магния
| Оксид магния | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Оксид магния |
| Традиционные названия | Жжёная магнезия, периклаз |
| Хим. формула | MgO |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 40,3044 г/моль |
| Плотность | 3,58 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 2825 °C |
| • кипения | 3600 °C |
| Энтальпия | |
| • образования | -601,8 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,0086 г/100мл (при 30°C)[1] |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Окси́д ма́гния (жжёная магнезия) — химическое соединение с формулой MgO, белые кристаллы, малорастворимые в воде, пожаро- и взрывобезопасен. Относится к классу основных оксидов. Основная форма — минерал периклаз.
Физические свойства
Легкий, рыхлый порошок белого цвета, легко впитывает воду. На этом свойстве основано его применение в спортивной гимнастике: нанесенный на ладони спортсмена, порошок предохраняет его от опасности сорваться с гимнастического снаряда. Температура плавления — 2825 °C. Температура кипения — 3600 °C. Плотность=3,58 г/см3.
Химические свойства
Реагирует с разбавленными кислотами с образованием солей, плохо — с холодной водой, образуя Mg(OH)2:
С горячей водой реагирует лучше, реакция идет быстрее.
- [math]\displaystyle{ \mathsf{MgO + 2HCl \rightarrow MgCl_2 + H_2O} }[/math]
- [math]\displaystyle{ \mathsf{MgO + H_2O \rightarrow Mg(OH)_2} }[/math]
Получение
Оксид магния получают обжигом минералов магнезита и доломита, а также брусита.
- [math]\ce{ CaCO3*MgCO3 -> MgO + CaO + 2CO2 }[/math]
- [math]\ce{ MgCO3 -> MgO + CO2 }[/math]
- [math]\ce{ Mg(OH)2 -> MgO + H2O }[/math]
Применение
В промышленности применяется для производства огнеупоров, цементов, очистки нефтепродуктов, как наполнитель при производстве резины, наполнитель в ТЭНах. Сверхлегкий оксид магния применяется как очень мелкий абразив для очистки поверхностей, в частности, в электронной промышленности.
В медицине применяют при повышенной кислотности желудочного сока, так как она обусловливается избыточным содержанием соляной кислоты. Жжёную магнезию принимают также при случайном попадании в желудок кислот.
В пищевой промышленности зарегистрирован в качестве пищевой добавки E530.
Является абсолютным отражателем — веществом с коэффициентом отражения, равным единице в широкой спектральной полосе. Может применяться как доступный эталон белого цвета.
См. также
Примечания
- ↑ Рабинович В. А., Хавин З. Я. «Краткий химический справочник». — Л.: Химия, 1978.
Литература
- Кнунянц И. Л. и др. т.2 Даффа-Меди // Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.