Нонагидридоренат(VII) натрия
| Нонагидридоренат(VII) натрия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Нонагидридоренат(VII) натрия |
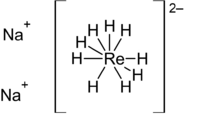
| Хим. формула | Na2[ReH9] |
| Физические свойства | |
| Состояние | бесцветные (белые) кристаллы |
| Молярная масса | 241,26 г/моль |
| Классификация | |
| SMILES | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нонагидридоренат(VII) натрия — неорганическое соединение, комплексный гидрид металлов натрия и рения с формулой Na2[ReH9], бесцветные (белые) кристаллы, растворимые в холодной воде, окисляется кислородом воздуха.
Получение
- При восстановлении перрената аммония натрием в этаноле:
- [math]\displaystyle{ \mathsf{NH_4ReO_4 + 18Na + 13C_2H_5OH \ \xrightarrow{}\ Na_2[ReH_9]\downarrow + 13C_2H_5ONa + 3NaOH + NH_3\cdot H_2O } }[/math]
Физические свойства
Нонагидридоренат(VII) натрия образует бесцветные (белые) кристаллы, хорошо растворимые в холодной воде, реагирует с горячей, окисляется кислородом воздуха.
Химические свойства
- Разлагается при нагревании:
- [math]\displaystyle{ \mathsf{2Na_2[ReH_9] \ \xrightarrow{245^oC}\ 4NaH + 2Re + 7H_2 } }[/math]
- Реагирует с горячей водой:
- [math]\displaystyle{ \mathsf{Na_2[ReH_9] + 5H_2O \ \xrightarrow{100^oC}\ NaReO_4 + NaOH + 9H_2 } }[/math]
- Реагирует с разбавленными кислотами:
- [math]\displaystyle{ \mathsf{2Na_2[ReH_9] + 4HCl \ \xrightarrow{}\ 4NaCl + 2Re\downarrow + 11H_2\uparrow } }[/math]
- Реагирует с горячей азотной кислотой:
- [math]\displaystyle{ \mathsf{4Na_2[ReH_9] + 22HNO_3 \ \xrightarrow{100^oC}\ 4NaReO_4 + 9NH_4NO_3 + 4NaNO_3 + 11H_2O } }[/math]
- Реагирует с горячей концентрированной перекисью водорода:
- [math]\displaystyle{ \mathsf{Na_2[ReH_9] + 9H_2O_2 \ \xrightarrow{100^oC}\ NaReO_4 + NaOH + 13H_2O } }[/math]
- Окисляется кислородом воздуха:
- [math]\displaystyle{ \mathsf{4Na_2[ReH_9] + 11O_2 \ \xrightarrow{\tau}\ 4Re + 8NaOH + 14H_2O } }[/math]
Литература
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.