Ацетилнитрат
Ацетилнитрат — бесцветная подвижная жидкость с формулой [math]\ce{ CH3COONO2 }[/math], реагент в реакциях нитрования[1].
Получение
Обычно ацетилнитрат получают медленным добавлением концентрированной азотной кислоты к охлаждённому уксусному ангидриду. К другим способам относятся растворение оксида азота(V) в уксусном ангидриде, реакция азотной кислоты и кетена, а также синтез in situ из ацетилхлорида и нитрата серебра в ацетонитриле[1].
Физические свойства
Ацетилнитрат обычно используют в виде смеси азотной кислоты и уксусного ангидрида. В свободном виде при нагревании он нестабилен и склонен ко взрыву (выше 100 °C). В растворе может взрываться при температуре выше 60 °C. Выделение или перегонка возможны только при соблюдении строгих мер безопасности. Ацетилнитрат растворим в распространённых органических растворителях[1][2].
Применение в органическом синтезе
Ацетилнитрат находит применение в органическом синтезе, в частности, в нитровании ароматических и некоторых неароматических соединений, в синтезе 2-нитроацетатов, а также в окислении органических сульфидов до сульфоксидов[1].
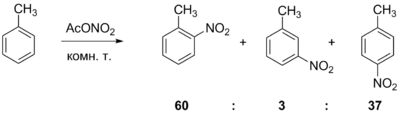
В реакциях электрофильного замещения ацетилнитрат проявляет себя как источник катионов нитрония [math]\ce{ NO2+ }[/math]. Так, при взаимодействии с толуолом и бифенилом он даёт соответствующие орто- и пара-нитросоединения, а в реакциях с нафталином и пиреном — 1-нитропроизводные. Также ацетилнитрат способен нитровать карбонильные соединения в енольной форме, например, ацетоуксусный эфир нитруется по активированному метиленовому звену[1].
Ацетилнитрат присоединяется по двойной связи простых алкенов, давая 2-нитроацетаты[1].

Также ацетилнитрат превращает спирты в соответствующие нитраты, а третичные амины — в нитрозамины. С органическими сульфидами ацетилнитрат реагирует весьма быстро, практически количественно давая сульфоксиды, причём дальнейшего окисления до сульфонов не наблюдается даже при избытке реагента[1].

Примечания
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 Louw R. Acetyl Nitrate (англ.) // e-EROS Encyclopedia of Reagents for Organic Synthesis. — Wiley, 2001. — doi:10.1002/047084289X.ra032.
- ↑ Acetyl Nitrate 591-09-3 // Sax's Dangerous Properties of Industrial Materials. — Wiley, 2004. — doi:10.1002/0471701343.sdp00346.
