Кетены

Кетены — соединения общей формулы R1R2C=C=O, в которых карбонильная группа соединена двойной связью с алкилиденовой группой[1]. Содержит кумулированную систему двойных связей C=C и C=O.
Номенклатура
Название кетенов R1R1C=C=O является производным от названия соответствующего основного соединения, например:
- H2C=C=O кетен
- (CH3)2C=C=O диметилкетен
Из кетенов R1R1C=C=O различают альдокетены (R1 = H, R2 — органический радикал) и кетокетены (R1, R2 — органические радикалы)
Физические свойства
Низшие гомологи ряда кетенов при нормальных условиях являются газами, следующие — желтоватыми жидкостями. Кетены растворимы в диэтиловом эфире, ароматических углеводородах и галогеноалканах.
Атомы углерода кетеновой группы находятся в состоянии sp2- и sp-гибридизации, сами кетены являются электрофильными реагентами, причём электрофильный центр располагается на атоме углерода в sp-гибридизованном состоянии
ИК-спектр кетенов имеет характеристические полосы в районе 2200, 2080 см-1.
Реакционная способность
Кетены малостабильны и являются высокореакционноспособными веществами, формально являющиеся внутренними ангидридами замещенных уксусных кислот и в реакциях с нуклеофилами выступающих в роли таких ангидридов:
- [math]\displaystyle{ \mathsf{R_2C\text{=}C\text{=}O + NuH \rightarrow R_2C\text{=}C(O^-)NuH^+ \rightarrow R_2CH\text{-}C(O)Nu} }[/math]
- Nu = ОН, ООН, OR, SR, NR2, RCOO, PR2
Альдокетены таутомерны инолам, однако равновесие полностью сдвинуто в сторону кетенной формы, вместе с тем, альдокетены под действием сильных оснований депротонируются с образованием нестабильных инолят-анионов[2]:
- (Me)3SiCH=C=O + n-BuLi [math]\displaystyle{ \to }[/math] (Me)3Si-C≡C-OLi + BuH
Кетены склонны вступать в реакции [2+2]-циклоприсоединения с соединениями с двойными связями: Так, жидкий кетен склонен к димеризации в дикетен:
Альдокетены аналогично димеризуются в β-алкилиден-β-лактоны (дикетены), кетодикетены димеризуются с образованием циклобутан-1,3-дионов.
Присоединение кетенов к иминам ведет к азетидин-2-онам (синтез β-лактамов по Штаудингеру):
Циклоприсоединение к алкенам ведет к образованию циклобутанонов, присоединение к алкинам - к циклобутенонам.
Кетены также вступают в реакции [2+1]-циклоприсоединения по связи C=C. Так, при взаимодействии кетенов с алифатическими диазосоединениями образуются циклопропаноны, сам дикетен при взаимодействии с диазометаном в растворе диэтилового эфира при -60 °C образует циклопропанон с выходом 75%; при присоединении диоксида серы к кетену образуется тииран-2-он-1,1-диоксид.
Некоторые дизамещенные кетены взаимодействуют с фосгеном или оксалилхлоридом, образуя дихлорангидриды дизамещенных малоновых кислот:
- Ph2C=C=O + (COCl)2 [math]\displaystyle{ \to }[/math] Ph2C(COCl)2 + CO
Получение и применение
В промышленности кетен получают пиролизом уксусной кислоты в присутствии триэтилфосфата или пиролизом ацетона над глинозёмом (Al2O3).

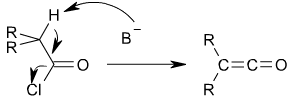
Лабораторный способ получения кетенов заключается в обработке хлорангидридов карбоновых кислот с атомом водорода в α-положении действием оснований, обычно третичных аминов. Выходы в случае хлорангидридов с достаточно подвижными α-атомами водорода велики, так например, хлорангидриды замещенных фенилуксусных кислот образуют кетены с выходами 61-78%[3]:
Также кетены могут быть синтезированы дегалогенированием галогенангидридов α-галогенкарбоновых кислот, так, например, хлорангидрид трихлоруксусной кислоты при действии цинковой пыли образует неустойчивый дихлоркетен[4]:
- CCl3COCl [math]\displaystyle{ \to }[/math] Cl2C=C=O
Кетены образуются в процессе перегруппировки Вольфа из α-диазокетонов:
и других α-диазокарбонильных соединений, например, тиоэфиров диазоуксуснной кислоты[5]:
- PhSCOCH=N=N [math]\displaystyle{ \to }[/math] PhSHC=C=O
Кетены применяются в органическом синтезе. В частности, кетен является ацетилирующим агентом для аминов, спиртов, енольных форм кетонов.
См. также
Примечания
- ↑ ketenes // IUPAC Gold Book. Дата обращения: 10 ноября 2011. Архивировано 20 октября 2012 года.
- ↑ (1978-01) «Reaction of trimethylsilylketene with strong base. Evidence for ketene enolate formation». The Journal of Organic Chemistry 43 (2): 376–376. doi:10.1021/jo00396a057. ISSN 0022-3263. Проверено 2020-10-20.
- ↑ Staudaher, Nicholas (2017). «Preparation of Aryl Alkyl Ketenes». Organic Syntheses 94: 1–15. doi:10.15227/orgsyn.094.0001. ISSN 23333553. Проверено 2020-10-19.
- ↑ (1990) «3-Butylcyclobutenone». Organic Syntheses 68: 32. doi:10.15227/orgsyn.068.0032. ISSN 00786209. Проверено 2020-10-19.
- ↑ Danheiser, Rick L. (2003). «Generation and [2+2 Cycloadditions of Thio-Substituted Ketenes: trans-1-(4-methoxyphenyl)-4-phenyl-3-(phenylthio)azetidin-2-one]». Organic Syntheses 80: 160. doi:10.15227/orgsyn.080.0160. ISSN 00786209. Проверено 2020-10-19.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2 (Даф-Мед). — 671 с. — ISBN 5-82270-035-5.
- О. Я. Нейланд. Органическая химия. — М.: Высшая школа, 1990. — 751 с. — 35 000 экз. — ISBN 5-06-001471-1.
- Danheiser, Rick L. Science of Synthesis: Houben-Weyl Methods of Molecular Transformations Vol. 23: Three Carbon-Heteroatom Bonds: Ketenes and Derivatives. — Georg Thieme Verlag, 2014-05-14. — ISBN 978-3-13-171971-3.