2-Хлорпропан
| Изопропилхлорид | |
|---|---|
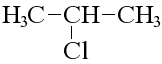  | |
| Общие | |
| Хим. формула | (CH3)2CHCl |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 78,541 г/моль |
| Плотность | 0.862 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | −117.18 °C |
| • кипения | 35.74 °C |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Изопропилхлорид или 2-хлорпропан (CH3)2CHCl — органическое соединение, представитель галогеналканов. Бесцветная легковоспламеняющаяся жидкость, со сладковатым запахом, малорастворимая в воде (до 0,45%), растворим в хлороформе, тетрахлорметане и бензоле, хуже растворим в диэтиловом эфире, тетрагидрофуране и ацетоне. Представляет собой изомер 1-хлорпропана.[1] В промышленности используется в органическом синтезе как растворитель.
Получение
2-Хлорпропан получают гидрогалогенированием пропена[1]
- [math]\ce{ CH2=CH-CH3 + HCl -> CH3-CH(Cl)-CH3 }[/math]
В лаборатории 2-xлорпропан может быть получен действием избытка концентрированной соляной кислоты на 2-пропанол в присутствии хлорида цинка с последующей отгонкой из реакционной смеси. [2]
- [math]\ce{ CH3-CH(OH)-CH3 + HCl ->[\ce{ZnCl2}] CH3-CH(Cl)-CH3 }[/math]
Жидкофазное фотохлорирование пропана даёт фракцию монохлорпропана содержащую 1-хлорпропан и 2-хлорпропан в соотношениях зависящих от температуры реакции( 52:48 при 30°С и 27:73 при 60°С). [1] При воздействии кислоты Льюиса происходит изомеризация 1-хлорпропана в 2-хлорпропан[3]:
- [math]\ce{ CH3-CH2-CH2Cl <=>[\ce{AlCl3}] CH3-CH(Cl)-CH3 }[/math]
Химические свойства
2-хорпропан может выступать алкилирующим агентом в реакции Фриделя-Крафтса. Так в присутствии хлорида алюминия он реагирует с бензолом. [4]

Для реакций O-изопропилирования[5] и N-изопропилирования[6] в лаборатории используют более дорогие, но более реакционноспособные 2-бром и 2-йодпропан.
Примечания
- ↑ 1,0 1,1 1,2 Изопропилхлорид - Большая Энциклопедия Нефти и Газа, статья, страница 1. www.ngpedia.ru. Дата обращения: 25 февраля 2020. Архивировано 25 февраля 2020 года.
- ↑ А. Мэррей, Д. Л. Уильямс. Синтезы органических соединений с изотопами водорода. М., ИЛ., 1961, стр. 227
- ↑ Курц А Л., Ливанцов М.В., Ливанцова Л.И. Электрофильное замещение в ароматическом ряду. Методическая разработка для студентов III курса. www.chem.msu.su (1997). Дата обращения: 12 апреля 2020. Архивировано 23 апреля 2020 года.
- ↑ Л. Титце, Т. Айхер. Препаративная органическая химия.Пер. с нем. под ред. д. х. н. Ю. Е. Алексеева.Москва, Мир, 1999, стр. 170
- ↑ Синтезы органических препаратов. Сборник 3.Москва, Иностранная Литература, 1952, стр. 135
- ↑ Методы получения химических реактивов и препаратов. Москва, ИРЕА, Выпуск 11, 1964, стр. 7