Вирус гепатита B
| Вирус гепатита B | |
|---|---|
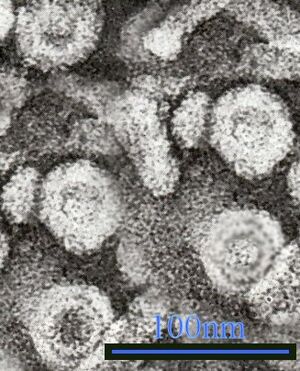 ПЭМ-микрофотография, показывающая вирионы вируса гепатита В | |
| Научная классификация | |
|
Реалм: Царство: Pararnavirae Тип: Artverviricota Класс: Порядок: Blubervirales Семейство: Вид: Вирус гепатита B |
|
| Международное научное название | |
| Hepatitis B virus | |
| Группа по Балтимору | |
| VII: дцДНК-ОТ-вирусы | |
Ви́рус гепати́та B (вирус гепатита b, «б»; англ. Hepatitis B virus, HBV) — ДНК-содержащий вирус из семейства гепаднавирусов, возбудитель вирусного гепатита B. В мире по различным оценкам от 3 до 6 % людей инфицировано вирусом гепатита B. Носительство вируса не обязательно сопровождается гепатитом, однако носитель вируса может заражать других людей, а также животных.
Болезнь
Несмотря на то, что существует вакцина для предотвращения гепатита В, вирус гепатита В остаётся глобальной проблемой здравоохранения. Гепатит В может протекать остро, а затем переходить в хроническую форму, приводя к другим заболеваниям и состояниям здоровья[2]. В дополнение к возникновению гепатита, заражение вирусом гепатита В может привести к циррозу и гепатоцеллюлярной карциноме[3].
Также было высказано предположение, что заболевание может увеличить риск возникновения рака поджелудочной железы[4].
Классификация
Вирус гепатита В классифицируется в роде Orthohepadnavirus, который содержит 11 других видов. Род классифицируется как часть семейства Hepadnaviridae, в которое входят четыре других рода: Avihepadnavirus, Herpetohepadnavirus, Metahepadnavirus and Parahepadnavirus[5]. Это семейство вирусов является единственным представителем вирусного отряда Blubervirales[5].
Вирусы, сходные с гепатитом В, были обнаружены у всех человекообразных обезьян (орангутанов, гиббонов, горилл и шимпанзе), у обезьян Старого Света[6], и у шерстистых обезьян Нового Света (вирус гепатита В шерстистых обезьян), что позволяет предположить древнее происхождение этого вируса у приматов.
Вирус подразделяется на четыре основных серотипа (adr, adw, ayr, ayw) на основе антигенных эпитопов, присутствующих на белках его оболочки. Эти серотипы основаны на общей детерминанте (a) и двух взаимоисключающих парах детерминант (d/y и w/r). Вирусные штаммы также были разделены на десять генотипов (A-J) и сорок подгенотипов в соответствии с общей вариацией нуклеотидной последовательности генома[7]. Генотипы имеют чёткое географическое распределение и используются для отслеживания эволюции и передачи вируса. Различия между генотипами влияют на тяжесть заболевания, течение и вероятность осложнений, и ответ на лечение[8][9]. Серотипы и генотипы не обязательно соответствуют.
Неклассифицированные виды
У летучих мышей выделен ряд пока ещё не классифицированных видов, подобных гепатиту В[10].
Морфология
Строение вирусной частицы

Вирус гепатита В является членом семейства гепаднавирусов[11]. Вирусная частица, называемая частицей Дейна[12] (вирион), состоит из внешней липидной оболочки и икосаэдрического ядра нуклеокапсида, состоящего из белка. Нуклеокапсид содержит вирусную ДНК и ДНК-полимеразу, которая обладает обратной транскриптазной активностью, подобной ретровирусам[13]. Внешняя оболочка содержит встроенные белки, которые участвуют в связывании вируса с восприимчивыми клетками и проникновении в них. Вирус является одним из самых маленьких оболочечных вирусов животных с диаметром вириона 42 нм, но также существуют плеоморфные формы, в том числе нитевидные и сферические тела, лишённые ядра. Эти частицы не являются инфекционными и состоят из липида и белка, которые образуют часть поверхности вириона, который называется поверхностным антигеном (HBsAg) и вырабатывается в избытке в течение жизненного цикла вируса[14].
Компоненты
Вирус состоит из:
- HBsAg (поверхностный антиген гепатита В) был первым обнаруженным белком вируса гепатита В[15]. Он состоит из малого (S), среднего (M) и большого (L) белка[16].
- HBcAg (основной антиген гепатита В) является основным структурным белком икосаэдрического нуклеокапсида HBV и участвует в репликации вируса. Образование капсида является основным фактором инфицирования клетки[17]. HBcAg способствует выведению HBV in vivo, но неизвестно, должен ли HBcAg находиться в форме капсида для содействия очистке от вируса[18].
- ДНК-полимераза вируса гепатита В включена в нуклеокапсид вместе с предгеномной РНК (pgRNA). Внутри капсида pgRNA подвергается обратной транскрипции, образуя (-) цепь ДНК. В то же время большая часть матрицы РНК разрушается под действием РНКазной активности полимеразы. За этим следует синтез (+) цепи ДНК, и полимераза в конечном итоге ковалентно связывается с (-) цепью ДНК[19][20]. Полимераза отбрасывается после того, как вирион заражает новую клетку.
- HBeAg (антиген оболочки гепатита В) может быть обнаружен между икосаэдрическим ядром нуклеокапсида и липидной оболочкой, но считается «неучастным» и секретируется и накапливается в сыворотке. HBeAg и HBcAg сделаны из одной и той же рамки считывания[21].
- HBx небольшой, длиной в 154 аминокислоты, неструктурный и играет важную роль в HBV-ассоциированном заболевании печени и в репликации HBV в клетках HepG2[22]. Многие виды активности были связаны с экспрессией HBx. Однако молекулярные механизмы многих из этих активностей неизвестны[23]. Этот белок является многофункциональным, он активирует клеточные сигнальные пути и необходим для вирусной инфекции[24].
Вирусу гепатита D требуются частицы оболочки HBV, чтобы стать вирулентными[25].
Эволюция
Раннюю эволюцию вируса гепатита B, как и всех других вирусов, трудно установить. Выявление гепаднавирусов у широкого круга позвоночных предполагает длительную коэволюцию. Идентификация эндогенных элементов hepadnaviridae, общих для различных видов птиц, показывает присутствие этого вируса у птиц в течение по меньшей мере 70 миллионов лет[26]. Хотя аналогичные доказательства отсутствуют для млекопитающих, филогенетическое положение ортогепаднавирусов как сестринской клады авигепаднавирусов предполагает присутствие вируса в предоках амниот и последующая коэволюция как с птицами, так и с млекопитающими после их расхождения (> 300 миллионов лет назад). Также было высказано предположение, что Новый мировой гепаднавирус летучих мышей может быть источником гепаднавирусов приматов[27]. У авихепаднавирусов отсутствует Х-белок, но в геноме утиного гепаднавируса присутствует рудиментарная Х-рамка считывания[28]. Х-белок, возможно, произошёл от ДНК-гликозилазы.
Недавно реконструкция геномов вируса гепатита В по древним человеческим останкам позволила более детально исследовать эволюцию этого вируса у людей[29][30][31]. В 2021 году исследование реконструировало 137 древних геномов вируса гепатита В и доказало присутствие вируса у людей, по крайней мере, с 10 000 лет[29]. Самый последний общий предок всех известных человеческих линий вируса гепатита В датируется от 20 000 до 12 000 лет назад. Однако нельзя сказать, присутствовал ли вирус у людей задолго до этого или был приобретён незадолго до этого от другого вида животных. Было показано, что эволюция вируса гепатита В у людей отражает известные события человеческой истории, такие как первое заселение Америки в позднем плейстоцене и переходный период неолита в Европе[29]. Эти исследования также показали, что некоторые древние штаммы вируса гепатита В все ещё заражают людей, в то время как другие вымерли[29][30][31]. Штаммы ВГВ, обнаруженные у африканских и Юго-восточноазиатских обезьян (шимпанзе, горилл, орангутанов и гиббонов), по-видимому, родственны человеческим штаммам ВГВ, что может отражать прошлые случаи межвидовой передачи[32][29].
Исследование изолятов из циркумполярной арктической человеческой популяции показало, что предок субгенотипа B5 (эндемичного типа, обнаруженного в этой популяции), что предковый вирус возник в Азии около 2000 лет назад (95 % HPD 900 г. до н. э. — 830 г. н. э.)[33]. Слияние произошло около 1000 г. н. э. Этот субгенотип распространился из Азии первоначально в Гренландию, а затем распространился на запад в течение последних 400 лет.
Строение генома
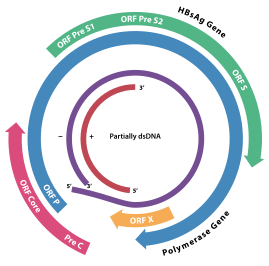
Размер
Геном вируса гепатита В состоит из кольцевой ДНК, но это необычно, потому что ДНК не является полностью двухцепочечной. Один конец полноразмерной цепи связан с вирусной ДНК-полимеразой. Длина генома составляет 3020-3320 нуклеотидов (для цепи полной длины) и 1700—2800 нуклеотидов (для короткой цепи)[34].
Кодирование
Отрицательная (некодирующая) цепь комплементарна вирусной мРНК. Вирусная ДНК обнаруживается в ядре вскоре после инфицирования клетки. Частично двухцепочечная ДНК становится полностью двухцепочечной путём завершения (+) смысловой цепи клеточными ДНК-полимеразами (вирусная ДНК−полимераза используется на более поздней стадии) и удаления белка вирусной полимеразы (P) из (-) смысловой цепи и короткой последовательности РНК из(+) смысловой нити. Некодирующие основания удаляются из концов (−) смысловой цепи, и концы соединяются.
Вирусные гены транскрибируются клеточной РНК-полимеразой II в ядре клетки с ковалентно замкнутой кольцевой ДНК (cccDNA). В геноме HBV были идентифицированы два усилителя, обозначенные как enhancer I (EnhI) и enhancer II (EnhII). Оба усилителя проявляют большую активность в клетках печёночного происхождения, и вместе они управляют и регулируют экспрессию полных вирусных транскриптов[35][36][37].
Существует четыре известных гена, кодируемых геномом, которые называются C, P, S и X. Основной белок кодируется геном C (HBcAg), и его стартовому кодону предшествует стартовый кодон AUG, из которого вырабатывается прекоординатный белок. HBeAg образуется в результате протеолитической переработки белка, предшествующего ядру. ДНК-полимераза кодируется геном P. Ген S — это ген, который кодирует поверхностный антиген (HBsAg). Ген HBsAg представляет собой одну длинную открытую рамку считывания, но содержит три «стартовых» (ATG) кодона в рамке, которые делят ген на три секции: pre-S1, pre-S2 и S. Из-за множества стартовых кодонов полипептиды трёх разных размеров называются большими, средними и малыми (pre-S2).-Вырабатываются S1 + pre-S2+ S, pre-S2+ S или S)[38].
Функция белка, кодируемого геном X, до конца не изучена[39], но некоторые данные свидетельствуют о том, что он может функционировать как транскрипционный трансактиватор. Интересно, что слитый белок с Х-ядром 40 кДа кодируется длинным вирусным транскриптом размером 3,9 кб, функция которого остаётся неясной[40]. Синтез 3.9 кб РНК инициируется в промоторной области гена X, и транскрипт полиаденилируется только после второго раунда транскрипции. Аналогичное поведение характерно и для других видов длинных прегеномных/предъядерных (pg/pc) РНК. Таким образом, механизм вирусной транскрипции должен игнорировать сигнал poly (A) на первом раунде транскрипции.
В геноме HBV было идентифицировано несколько некодирующих элементов РНК. К ним относятся: HBV PREalpha, HBV PREbeta и сигнал инкапсидации РНК HBV epsilon[41][42].
Генотипы
Известно восемь генотипов, обозначенных от А до H[8]. Был описан возможный новый генотип «I»[43], но принятие этого обозначения не является универсальным[44].
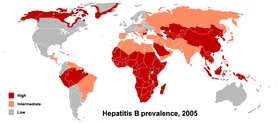
Различия между генотипами составляют более 8 %. Генотипы A и D распространены повсеместно; генотипы C и B характерны для Юго-Восточной Азии и Японии. Генотип Е распространён преимущественно в Африке. Генотип F был найден среди коренного населения Южной Америки и на Аляске. Генотип G спорадически встречается в различных частях света, в частности в Соединённых Штатах Америки и во Франции. Генотипы Е и G характеризуются низкой вариабельностью в последовательности нуклеотидов в геноме, по сравнению с другими генотипами.
Генотипы вируса гепатита B могут обладать различными биологическими свойствами. В последнее время все большое значение придаётся генотипу вируса в клинических аспектах течения вирусной инфекции, а также чувствительности к антивирусным препаратам. На сегодняшний день установлено, что инфекция, вызванная вирусом гепатита B генотипов В и С, коррелирует с повреждением печени; а инфекция, обусловленная вирусом гепатита B генотипа А, эффективно излечивается терапевтическими методами с использованием интерферона.
Генотип D имеет 10 подгенотипов[45][7].
Репликация вируса

Жизненный цикл вируса гепатита В сложен. Гепатит В является одним из немногих известных неретровирусных вирусов, которые используют обратную транскрипцию как часть процесса репликации.
- Присоединение
- Вирус проникает в клетку путём связывания с рецепторами на поверхности клетки и проникает в неё путём эндоцитоза, опосредованного либо клатрином, либо кавеолином-1[46]. ВГВ первоначально связывается с протеогликаном гепаринсульфата. Сегмент pre-S1 белка HBV L затем плотно связывается с котранспортирующим полипептидом тауроколата натрия (NTCP), кодируемым геном slc10a1[47]. NTCP в основном обнаруживается в синусоидальной мембране клеток печени. Присутствие NTCP в клетках печени коррелирует с тканевой специфичностью инфекции ВГВ[46].
- Проникновение
- После эндоцитоза мембрана вируса сливается с мембраной клетки-хозяина, высвобождая нуклеокапсид в цитоплазму[48].
Снятие покрытия
- Поскольку вирус размножается с помощью РНК, вырабатываемой ферментом хозяина, вирусная геномная ДНК должна быть перенесена в ядро клетки. Считается, что капсид транспортируется по микротрубочкам к ядерной поре. Основные белки диссоциируют от частично двухцепочечной вирусной ДНК, которая затем становится полностью двухцепочечной (ДНК-полимеразами хозяина) и превращается в ковалентно замкнутую кольцевую ДНК (cccDNA), которая служит матрицей для транскрипции четырёх вирусных мРНК.
- Репликация
- Самая большая мРНК (которая длиннее вирусного генома) используется для создания новых копий генома и для производства белка капсидного ядра и вирусной РНК-зависимой ДНК-полимеразы.
- Сборка
- Эти четыре вирусных транскрипта подвергаются дополнительной обработке и продолжают образовывать вирионы-потомки, которые высвобождаются из клетки или возвращаются в ядро и повторно проходят цикл для получения ещё большего количества копий[38][49].
- Высвобождение
- Затем длинная мРНК транспортируется обратно в цитоплазму, где белок вириона Р синтезирует ДНК посредством своей обратно-транскриптазной активности.
Трансактивированные гены
HBV обладает способностью трансактивировать FAM46A[50].
Профилактика
Упомянутый выше поверхностный HBsAg-антиген, находящийся в наружной оболочке, применяют для производства высокоэффективной профилактической вакцины.
См. также
Примечания
- ↑ Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV).
- ↑ (2019) «Revisiting Hepatitis B Virus: Challenges of Curative Therapies». Journal of Virology 93 (20). doi:10.1128/JVI.01032-19. PMID 31375584.
- ↑ (March 2008) «Solution structure of stem-loop alpha of the hepatitis B virus post-transcriptional regulatory element». Nucleic Acids Research 36 (5): 1681–9. doi:10.1093/nar/gkn006. PMID 18263618.
- ↑ (October 2008) «Association between hepatitis B virus and pancreatic cancer». Journal of Clinical Oncology 26 (28): 4557–62. doi:10.1200/JCO.2008.17.3526. PMID 18824707.
- ↑ 5,0 5,1 ICTV Report Hepadnaviridae.
- ↑ (November 2013) «Discovery of naturally occurring transmissible chronic hepatitis B virus infection among Macaca fascicularis from Mauritius Island.». Hepatology 58 (5): 1610–1620. doi:10.1002/hep.26428. PMID 23536484.
- ↑ 7,0 7,1 (February 2017) «A novel hepatitis B virus subgenotype D10 circulating in Ethiopia». Journal of Viral Hepatitis 24 (2): 163–173. doi:10.1111/jvh.12631. PMID 27808472.
- ↑ 8,0 8,1 (March 2005) «Hepatitis B virus genotypes». Vaccine 23 (19): 2409–23. doi:10.1016/j.vaccine.2004.10.045. PMID 15752827.
- ↑ (1995) «Subtypes, genotypes and molecular epidemiology of the hepatitis B virus as reflected by sequence variability of the S-gene». Intervirology 38 (1–2): 24–34. doi:10.1159/000150411. PMID 8666521.
- ↑ (October 2013) «Bats carry pathogenic hepadnaviruses antigenically related to hepatitis B virus and capable of infecting human hepatocytes». Proceedings of the National Academy of Sciences of the United States of America 110 (40): 16151–6. doi:10.1073/pnas.1308049110. PMID 24043818. .
- ↑ Zuckerman AJ. Chapter 70: Hepatitis Viruses // Baron's Medical Microbiology / Baron S. — 4th. — Univ of Texas Medical Branch, 1996. — ISBN 978-0-9631172-1-2.
- ↑ WHO | Hepatitis B. www.who.int. Дата обращения: 12 июля 2015. Архивировано 10 июля 2015 года.
- ↑ (2004) «Molecular virology of hepatitis B virus». Seminars in Liver Disease 24 Suppl 1 (Suppl 1): 3–10. doi:10.1055/s-2004-828672. PMID 15192795.
- ↑ (July 1986) «The biology of hepadnaviruses». The Journal of General Virology 67 (7): 1215–35. doi:10.1099/0022-1317-67-7-1215. PMID 3014045.
- ↑ (April 2010) «Hepatitis B surface antigen (HBsAg) levels in the natural history of hepatitis B virus (HBV)-infection: a European perspective». Journal of Hepatology 52 (4): 514–22. doi:10.1016/j.jhep.2010.01.014. PMID 20207438.
- ↑ (March 2000) «Hepatitis B virus biology». Microbiology and Molecular Biology Reviews 64 (1): 51–68. doi:10.1128/mmbr.64.1.51-68.2000. PMID 10704474.
- ↑ (May 2010) «Hepatitis B virus core antigen determines viral persistence in a C57BL/6 mouse model». Proceedings of the National Academy of Sciences of the United States of America 107 (20): 9340–5. doi:10.1073/pnas.1004762107. PMID 20439715. .
- ↑ (March 2009) «A mutant hepatitis B virus core protein mimics inhibitors of icosahedral capsid self-assembly». Biochemistry 48 (8): 1736–42. doi:10.1021/bi801814y. PMID 19196007.
- ↑ (October 2014) «Nucleoside/nucleotide analog inhibitors of hepatitis B virus polymerase: mechanism of action and resistance». Current Opinion in Virology 8: 1–9. doi:10.1016/j.coviro.2014.04.005. PMID 24814823.
- ↑ (September 2014) «Persistence of hepatitis B virus covalently closed circular DNA in hepatocytes: molecular mechanisms and clinical significance». Emerging Microbes & Infections 3 (9): e64. doi:10.1038/emi.2014.64. PMID 26038757.
- ↑ TSRI - News and Publications. Дата обращения: 3 января 2009.
- ↑ (October 2006) «Molecular functions and biological roles of hepatitis B virus x protein». Cancer Science 97 (10): 977–83. doi:10.1111/j.1349-7006.2006.00299.x. PMID 16984372.
- ↑ (November 2007) «Hepatitis B virus replication is associated with an HBx-dependent mitochondrion-regulated increase in cytosolic calcium levels». Journal of Virology 81 (21): 12061–5. doi:10.1128/JVI.00740-07. PMID 17699583.
- ↑ (July 2003) «Activation and inhibition of cellular calcium and tyrosine kinase signaling pathways identify targets of the HBx protein involved in hepatitis B virus replication». Journal of Virology 77 (14): 7713–9. doi:10.1128/JVI.77.14.7713-7719.2003. PMID 12829810.
- ↑ (August 2008) «Properties of subviral particles of hepatitis B virus». Journal of Virology 82 (16): 7812–7. doi:10.1128/JVI.00561-08. PMID 18524834.
- ↑ (2013-04-30) «The genome of a Mesozoic paleovirus reveals the evolution of hepatitis B viruses» (en). Nature Communications 4 (1): 1791. doi:10.1038/ncomms2798. ISSN 2041-1723. PMID 23653203. .
- ↑ (February 2016) «Bat hepadnaviruses and the origins of primate hepatitis B viruses». Current Opinion in Virology 16: 86–94. doi:10.1016/j.coviro.2016.01.015. PMID 26897577.
- ↑ (2000) «A vestigial X open reading frame in duck hepatitis B virus». Intervirology 43 (3): 185–90. doi:10.1159/000025037. PMID 11044813.
- ↑ 29,0 29,1 29,2 29,3 29,4 (2021-10-08) «Ten millennia of hepatitis B virus evolution» (EN). Science 374 (6564): 182–188. doi:10.1126/science.abi5658. PMID 34618559. .
- ↑ 30,0 30,1 (May 2018) «Ancient hepatitis B viruses from the Bronze Age to the Medieval period». Nature 557 (7705): 418–423. doi:10.1038/s41586-018-0097-z. PMID 29743673. .
- ↑ 31,0 31,1 (2018-05-10) «Neolithic and medieval virus genomes reveal complex evolution of hepatitis B». eLife 7: e36666. doi:10.7554/eLife.36666. ISSN 2050-084X. PMID 29745896.
- ↑ (March 2013) «Dating the origin and dispersal of hepatitis B virus infection in humans and primates». Hepatology 57 (3): 908–16. doi:10.1002/hep.26079. PMID 22987324.
- ↑ (2017) «Tracing hepatitis B virus (HBV) genotype B5 (formerly B6) evolutionary history in the circumpolar Arctic through phylogeographic modelling». PeerJ 5: e3757. doi:10.7717/peerj.3757. PMID 28875087.
- ↑ (August 2007) «Hepatitis B virus genetic variability and evolution». Virus Research 127 (2): 164–76. doi:10.1016/j.virusres.2007.02.021. PMID 17383765.
- ↑ (February 2004) «Enhancer I predominance in hepatitis B virus gene expression». Molecular and Cellular Biology 24 (4): 1799–808. doi:10.1128/mcb.24.4.1799-1808.2004. PMID 14749394.
- ↑ (February 1989) «Hepatitis B virus (HBV) promoters are regulated by the HBV enhancer in a tissue-specific manner». Journal of Virology 63 (2): 579–83. doi:10.1128/JVI.63.2.579-583.1989. PMID 2536093.
- ↑ (1993) «Regulation of hepatitis B virus gene expression». Journal of Hepatology 17 Suppl 3: S20-3. doi:10.1016/s0168-8278(05)80419-2. PMID 8509635.
- ↑ 38,0 38,1 (January 2007) «Hepatitis B virus replication». World Journal of Gastroenterology 13 (1): 48–64. doi:10.3748/wjg.v13.i1.48. PMID 17206754.
- ↑ (December 2004) «The enigmatic X gene of hepatitis B virus». Journal of Virology 78 (23): 12725–34. doi:10.1128/JVI.78.23.12725-12734.2004. PMID 15542625.
- ↑ (May 2003) «A long HBV transcript encoding pX is inefficiently exported from the nucleus» (en). Virology 309 (2): 339–349. doi:10.1016/S0042-6822(03)00156-9. PMID 12758180.
- ↑ (November 1998) «The hepatitis B virus post-transcriptional regulatory element contains two conserved RNA stem-loops which are required for function». Nucleic Acids Research 26 (21): 4818–27. doi:10.1093/nar/26.21.4818. PMID 9776740.
- ↑ (November 2002) «The apical stem-loop of the hepatitis B virus encapsidation signal folds into a stable tri-loop with two underlying pyrimidine bulges». Nucleic Acids Research 30 (21): 4803–11. doi:10.1093/nar/gkf603. PMID 12409471.
- ↑ (November 2008) «Possible new hepatitis B virus genotype, southeast Asia». Emerging Infectious Diseases 14 (11): 1777–80. doi:10.3201/eid1411.080437. PMID 18976569.
- ↑ (August 2008) «When should "I" consider a new hepatitis B virus genotype?». Journal of Virology 82 (16): 8241–2. doi:10.1128/JVI.00793-08. PMID 18663008.
- ↑ (March 2013) «New HBV subgenotype D9, a novel D/C recombinant, identified in patients with chronic HBeAg-negative infection in Eastern India». Journal of Viral Hepatitis 20 (3): 209–18. doi:10.1111/j.1365-2893.2012.01655.x. PMID 23383660.
- ↑ 46,0 46,1 (July 2016) «Visualization of hepatitis B virus entry - novel tools and approaches to directly follow virus entry into hepatocytes». FEBS Letters 590 (13): 1915–26. doi:10.1002/1873-3468.12202. PMID 27149321.
- ↑ (September 2015) «NTCP opens the door for hepatitis B virus infection». Antiviral Research 121: 24–30. doi:10.1016/j.antiviral.2015.06.002. PMID 26071008.
- ↑ (August 2015) «Hepatitis B Virus and Hepatitis D Virus Entry, Species Specificity, and Tissue Tropism». Cold Spring Harbor Perspectives in Medicine 5 (8): a021378. doi:10.1101/cshperspect.a021378. PMID 26238794.
- ↑ (January 2007) «Hepatitis B virus morphogenesis». World Journal of Gastroenterology 13 (1): 65–73. doi:10.3748/wjg.v13.i1.65. PMID 17206755.
- ↑ Fam46A (Protein Coding). GeneCards. GeneCards. Дата обращения: 18 февраля 2015.