Серная кислота
| Серная кислота | |
|---|---|
   | |
 | |
| Общие | |
| Систематическое наименование |
Серная кислота |
| Традиционные названия | Серная кислота, купоросное масло, олеум |
| Хим. формула | H2SO4 |
| Рац. формула | H2SO4 |
| Физические свойства | |
| Состояние | Жидкость |
| Молярная масса | 98,078 ± 0,006 г/моль |
| Плотность | 1,8356 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | +10,38 °C |
| • кипения | +337 °C |
| • разложения | +450 °C |
| Удельная теплота плавления | 10,73 Дж/кг |
| Химические свойства | |
| Константа диссоциации кислоты [math]\displaystyle{ pK_a }[/math] | -3 |
| Растворимость | |
| • в воде | Растворима |
| Оптические свойства | |
| Показатель преломления | 1.397 |
| Структура | |
| Дипольный момент | 2.72 Д |
| Классификация | |
| Рег. номер CAS | 7664-93-9 |
| PubChem | 1118 |
| Рег. номер EINECS | 231-639-5 |
| RTECS | WS5600000 |
| Безопасность | |
| Предельная концентрация | 1 мг/м3 |
| ЛД50 | 100 мг/кг |
| Токсичность | 2-й класс опасности[1], общетоксическое действие. |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Се́рная кислота́ (химическая формула — H2SO4) — сильная неорганическая кислота, отвечающая высшей степени окисления серы (+6).
При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха, с сильнокислым «медным» вкусом. В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Если молярное отношение SO3 : H2O < 1, то это водный раствор серной кислоты, если > 1 — раствор SO3 в серной кислоте (олеум). Токсична в больших дозах[2], обладает исключительно сильной коррозионной активностью.
Название
В XVIII—XIX веках серу для пороха производили из серного колчедана (пирит) на купоросных заводах. Серную кислоту в то время называли «купоросным маслом»[3][4], очевидно отсюда происхождение названия её солей (а точнее именно кристаллогидратов) — купоросы.
Исторические сведения
Серная кислота известна с древности, встречаясь в природе в свободном виде, например, в виде озёр вблизи вулканов. Возможно, первое упоминание о кислых газах, получаемых при прокаливании квасцов или железного купороса «зеленого камня», встречается в сочинениях, приписываемых арабскому алхимику Джабир ибн Хайяну.
В IX веке персидский алхимик Ар-Рази, прокаливая смесь железного и медного купороса (FeSO4•7H2O и CuSO4•5H2O), также получил раствор серной кислоты. Этот способ усовершенствовал европейский алхимик Альберт Магнус, живший в XIII веке.
Схема получения серной кислоты из железного купороса — термическое разложение сульфата железа (II) с последующим охлаждением смеси[5]

- [math]\displaystyle{ \mathsf{4FeSO_4 \xrightarrow{} 2Fe_2O_3+4SO_2\uparrow+O_2\uparrow} }[/math]
- [math]\displaystyle{ \mathsf{2SO_2+2H_2O+O_2 \rightleftarrows 2H_2SO_4} }[/math]
В трудах алхимика Валентина (XIII в) описывается способ получения серной кислоты путём поглощения водой газа (серный ангидрид), выделяющегося при сжигании смеси порошков серы и селитры. Впоследствии этот способ лег в основу т. н. «камерного» способа, осуществляемого в небольших камерах, облицованных свинцом, который не растворяется в серной кислоте. В СССР такой способ просуществовал вплоть до 1955 г.
Алхимикам XV века в известен был также способ получения серной кислоты из пирита — серного колчедана, более дешёвого и распространенного сырья, чем сера. Таким способом получали серную кислоту на протяжении 300 лет, небольшими количествами в стеклянных ретортах. Впоследствии, в связи с развитием катализа этот метод вытеснил камерный способ синтеза серной кислоты. В настоящее время серную кислоту получают каталитическим окислением (на V2O5) оксида серы (IV) в оксид серы (VI), и последующим растворением оксида серы (VI) в 70 % серной кислоте с образованием олеума.
В России производство серной кислоты впервые было организовано в 1805 году под Москвой в Звенигородском уезде. В 1913 году Россия по производству серной кислоты занимала 13 место в мире.[6]
Физические и физико-химические свойства
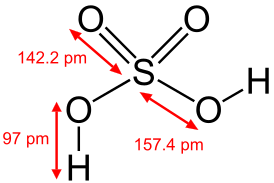
Серная кислота — это очень сильная двухосновная кислота, при 18оС pKa (1) = −2,8, pKa (2) = 1,92 (К₂ 1,2 10−2); длины связей в молекуле S=O 0,143 нм, S—OH 0,154 нм, угол HOSOH 104°, OSO 119°; кипит, образуя азеотропную смесь (98,3 % H2SO4 и 1,7 % H2О с температурой кипения 338,8оС). Смешивается с водой и SO3, во всех соотношениях. В водных растворах серная кислота практически полностью диссоциирует на H3О+, HSO3+, и 2НSO₄−. Образует гидраты H2SO4·nH2O, где n = 1, 2, 3, 4 и 6,5.
| H2SO4 | HSO4− | H3SO4+ | H3O+ | HS2O7⁻ | H2S2O7 | |
| состав, % | 99,5 | 0,18 | 0,14 | 0,09 | 0,05 | 0,04 |
Олеум
Растворы серного ангидрида SO3 в серной кислоте называются олеумом, они образуют два соединения H2SO4·SO3 и H2SO4·2SO3.
Олеум содержит также пиросерные кислоты, образующиеся по реакциям:
- [math]\displaystyle{ \mathsf{H_2SO_4 + SO_3 \rightarrow H_2S_2O_7} ; }[/math] Сульфит
- [math]\displaystyle{ \mathsf{H_2SO_4 + 2SO_3 \rightarrow H_2S_3O_{10}} . }[/math]
Температура кипения водных растворов серной кислоты повышается с ростом её концентрации и достигает максимума при содержании 98,3 % H2SO4.
| Содержание % по массе | Плотность при 20 °C, г/см3 | Температура плавления, °C | Температура кипения, °C | |
|---|---|---|---|---|
| H2SO4 | SO3 (свободный) | |||
| 10 | - | 1,0661 | −5,5 | 102,0 |
| 20 | - | 1,1394 | −19,0 | 104,4 |
| 40 | - | 1,3028 | −65,2 | 113,9 |
| 60 | - | 1,4983 | −25,8 | 141,8 |
| 80 | - | 1,7272 | −3,0 | 210,2 |
| 98 | - | 1,8365 | 0,1 | 332,4 |
| 100 | - | 1,8305 | 10,4 | 296,2 |
| 104,5 | 20 | 1,8968 | −11,0 | 166,6 |
| 109 | 40 | 1,9611 | 33,3 | 100,6 |
| 113,5 | 60 | 2,0012 | 7,1 | 69,8 |
| 118,0 | 80 | 1,9947 | 16,9 | 55,0 |
| 122,5 | 100 | 1,9203 | 16,8 | 44,7 |
Температура кипения олеума с увеличением содержания SO3 понижается. При увеличении концентрации водных растворов серной кислоты общее давление пара над растворами понижается и при содержании 98,3 % H2SO4 достигает минимума. С увеличением концентрации SO3 в олеуме общее давление пара над ним повышается. Давление пара над водными растворами серной кислоты и олеума можно вычислить по уравнению:
- [math]\displaystyle{ \lg p\ {{=}}\ \rm {A}\ {{-}}\ {B \over \it {T}}\ {{+}}\ 2{,}126{,} }[/math]
величины коэффициентов А и В зависят от концентрации серной кислоты. Пар над водными растворами серной кислоты состоит из смеси паров воды, H2SO4 и SO3, при этом состав пара отличается от состава жидкости при всех концентрациях серной кислоты, кроме соответствующей азеотропной смеси.
С повышением температуры усиливается диссоциация:
- [math]\displaystyle{ \mathsf{H_2SO_4 \lt =\gt SO_3 + H_2O - Q} . }[/math]
Уравнение температурной зависимости константы равновесия:
- [math]\displaystyle{ \ln {\it {K_p}} = 14{,}74965 - 6{,}71464 \ln {298 \over \it {T}} - 8{,}10161 \cdot 10^4 \it {T^2} - {\rm 9643{,}04 \over \it {T}} - \rm 9{,}4577 \cdot 10^{-3} \it {T} + \rm 2{,}19062 \cdot 10^{-6}\it {T^2}. }[/math]
При нормальном давлении степень диссоциации: 10−5 (373 К), 2,5 (473 К), 27,1 (573 К), 69,1 (673 К).
Плотность 100%-ной серной кислоты можно определить по уравнению:
- [math]\displaystyle{ d = 1{,}8517 - 1{,}1 \cdot 10^{-3} t + 2 \cdot 10^{-6} t^2. }[/math]
С повышением концентрации растворов серной кислоты их теплоемкость уменьшается и достигает минимума для 100%-ной серной кислоты, теплоемкость олеума с повышением содержания SO3 увеличивается.
При повышении концентрации и понижении температуры теплопроводность λ уменьшается:
- [math]\displaystyle{ \lambda = 0{,}518 + 0{,}0016 t - (0{,}25 + t/1293)\cdot C/ 100, }[/math]
где С — концентрация серной кислоты, в %.
Максимальную вязкость имеет олеум H2SO4·SO3, с повышением температуры η снижается. Для олеума минимальное ρ при концентрации 10 % SO3. С повышением температуры ρ серной кислоты увеличивается. Диэлектрическая проницаемость 100%-ной серной кислоты 101 (298,15 К), 122 (281,15 К); криоскопическая постоянная 6,12, эбулиоскопическая постоянная 5,33; коэффициент диффузии пара серной кислоты в воздухе изменяется в зависимости от температуры; D = 1,67·10−5T3/2 см2/с.
| ω, % | 5 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 85 | 86 | 87 | 88 | 89 | 90 | 91 | 92 | 93 | 94 | 95 | 96 | 97 | 98 | 99 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ρ H2SO4, г/мл | 1,03 | 1,064 | 1,1365 | 1,215 | 1,2991 | 1,3911 | 1,494 | 1,6059 | 1,7221 | 1,7732 | 1,7818 | 1,7897 | 1,7968 | 1,8033 | 1,8091 | 1,8142 | 1,8188 | 1,8227 | 1,826 | 1,8286 | 1,8305 | 1,8314 | 1,831 | 1,8292 | 1,8255 |
Химические свойства
Серная кислота в концентрированном виде при нагревании — довольно сильный окислитель.
1. Окисляет HI и частично HBr до свободных галогенов:
Углерод до CO2, серу — до SO2.
- [math]\displaystyle{ \mathsf{C + 2H_2SO_4 = 2SO_2\uparrow + CO_2\uparrow + 2H_2O} }[/math]
- [math]\displaystyle{ \mathsf{S + 2H_2SO_4 = 3SO_2\uparrow + 2H_2O} }[/math]
2. Окисляет многие металлы (исключения: Au, Pt, Ir, Rh, Ta). При этом концентрированная серная кислота восстанавливается до диоксида серы, например[10]:
- [math]\displaystyle{ \mathsf{Cu + 2H_2SO_4 = CuSO_4 + 2H_2O+SO_2\uparrow} }[/math]
3. На холоде в концентрированной серной кислоте Fe, Al, Cr, Co, Ni, Ba пассивируются, и реакции не протекают.
Наиболее сильными восстановителями концентрированная серная кислота восстанавливается до серы и сероводорода. Концентрированная серная кислота поглощает водяные пары, поэтому она применяется для сушки газов, жидкостей и твёрдых тел, например, в эксикаторах. Однако концентрированная H2SO4 частично восстанавливается водородом, из-за чего не может применяться для его сушки. Отщепляя воду от органических соединений и оставляя при этом чёрный углерод (уголь), концентрированная серная кислота приводит к обугливанию древесины, сахара и других веществ[10].
4. Разбавленная H2SO4 взаимодействует со всеми металлами, находящимися в электрохимическом ряду напряжений левее водорода с его выделением, например[10]:
- [math]\displaystyle{ \mathsf{Fe + H_2SO_4 = FeSO_4 + H_2{\uparrow}} }[/math]
5. Окислительные свойства для разбавленной H2SO4 нехарактерны. Серная кислота образует два ряда солей: средние — сульфаты и кислые — гидросульфаты, а также эфиры. Известны пероксомоносерная (или кислота Каро) H2SO5 и пероксодисерная H2S2O8 кислоты.
- [math]\displaystyle{ \mathsf{H_2SO_4 + 2NaOH = Na_2SO_4 + 2H_2O} }[/math]
6. Серная кислота реагирует с основными оксидами, образуя сульфат металла и воду:
- [math]\displaystyle{ \mathsf{CuO + H_2SO_4 = CuSO_4 + H_2O} }[/math]
7. На металлообрабатывающих заводах раствор серной кислоты применяют для удаления слоя оксида металла с поверхности металлических изделий, подвергающихся в процессе изготовления сильному нагреванию. Так, оксид железа удаляется с поверхности листового железа действием нагретого раствора серной кислоты:
- [math]\displaystyle{ \mathsf{Fe_2O_3 + 3H_2SO_4 = Fe_2 (SO_4)_3 + 3H_2O} }[/math]
8. Концентрированная H2SO4 превращает некоторые органические вещества в другие соединения углерода:
- [math]\displaystyle{ \mathsf{HCOOH + H_2SO_4(k) = CO\uparrow + H_2SO_4 \cdot nH_2O} }[/math]
9. Качественная реакция на серную кислоту и её растворимые соли — это их взаимодействие с растворимыми солями бария, при котором образуется белый осадок сульфата бария, нерастворимый в воде и кислотах, например[11]:
- [math]\displaystyle{ \mathsf{H_2SO_4+BaCl_2=BaSO_4{\downarrow}+2HCl{\uparrow}} }[/math]
Получение серной кислоты
Промышленный (контактный) способ
В промышленности серную кислоту получают окислением диоксида серы (сернистый газ, образующийся в процессе сжигания элементарной серы, серного колчедана или сероводород-содержащих газов, поступающих с установок гидроочистки и систем отпарки кислых стоков) до триоксида (серного ангидрида) на твёрдом ванадиевом катализаторе в четыре ступени (данная реакция экзотермична, поэтому применяется промежуточное охлаждение после первого слоя с помощью трубных пучков, через которые подаётся воздух, и после следующих двух ступеней — с помощью кольцевой трубы, имеющей большой диаметр, через которую подаётся воздух, над которой расположен дефлектор. Воздух нагнетается воздуходувками, часть горячего воздуха подаётся на горелочные устройства котлов, в которых производится сжигание сероводородсодержащих газов) последующим охлаждением и взаимодействием SO3 с водой. Получаемую данным способом серную кислоту также называют «контактной» (концентрация 92-94 %).
- [math]\displaystyle{ \mathsf{2SO_2 + O_2 = 2SO_3} }[/math]
- [math]\displaystyle{ \mathsf{H_2O + SO_3 = H_2SO_4} }[/math]
Нитрозный (башенный) способ
Раньше серную кислоту получали исключительно нитрозным методом в специальных башнях, а кислоту называли «башенной» (концентрация 75 %). Сущность этого метода заключается в окислении диоксида серы диоксидом азота в присутствии воды. Именно таким способом произошла реакция в воздухе Лондона во время Великого смога.
- [math]\displaystyle{ \mathsf{SO_2 + NO_2 + H_2O = H_2SO_4 + NO\uparrow} }[/math]
Лабораторные методы
В лаборатории можно получить серную кислоту взаимодействием сероводорода, элементарной серы и диоксида серы с хлорной или бромной водой или пероксидом водорода:
[math]\displaystyle{ \mathsf {H_2S + 4Br_2 + 4H_2O = H_2SO_4 + 8HBr\uparrow} }[/math]
[math]\displaystyle{ \mathsf{S + 3Br_2 + 4H_2O = H_2SO_4 + 6HBr\uparrow} }[/math]
[math]\displaystyle{ \mathsf{SO_2 + Br_2 + 2H_2O = H_2SO_4 + 2HBr\uparrow} }[/math]
[math]\displaystyle{ \mathsf {H_2S + 4Cl_2 + 4H_2O = H_2SO_4 + 8HCl\uparrow} }[/math]
[math]\displaystyle{ \mathsf{S + 3Cl_2 + 4H_2O = H_2SO_4 + 6HCl\uparrow} }[/math]
[math]\displaystyle{ \mathsf{SO_2 + Cl_2 + 2H_2O = H_2SO_4 + 2HCl\uparrow} }[/math]
[math]\displaystyle{ \mathsf{H_2S + 4H_2O_2 = H_2SO_4 + 4H_2O} }[/math]
[math]\displaystyle{ \mathsf{S + 3H_2O_2 = H_2SO_4 + 2H_2O} }[/math]
[math]\displaystyle{ \mathsf{SO_2 + H_2O_2 = H_2SO_4} }[/math]
Также её можно получить взаимодействием диоксида серы с кислородом и водой при +70°C под давлением в присутствии сульфата меди (II):
[math]\displaystyle{ \mathsf{2SO_2 +2H_2O + O_2 \ \xrightarrow {+70^oC, p, CuSO_4}\ 2H_2SO_4} }[/math]
Применение


Серную кислоту применяют:
- в обработке руд, особенно при добыче редких элементов, в том числе урана, иридия, циркония, осмия и т. п.;
- в производстве минеральных удобрений;
- в качестве электролита в свинцовых аккумуляторах;
- для получения различных минеральных кислот и солей;
- в производстве химических волокон, красителей, дымообразующих и взрывчатых веществ;
- в нефтяной, металлообрабатывающей, текстильной, кожевенной и др. отраслях промышленности;
- в пищевой промышленности — зарегистрирована в качестве пищевой добавки E513 (эмульгатор);
- в промышленном органическом синтезе в реакциях:
- дегидратации (получение диэтилового эфира, сложных эфиров);
- гидратации (этанола из этилена);
- сульфирования (синтетические моющие средства и промежуточные продукты в производстве красителей);
- алкилирования (получение изооктана, полиэтиленгликоля, капролактама) и др.;
- восстановления смол в фильтрах на производстве дистиллированной воды.
Мировое производство серной кислоты около 200 млн тонн в год[12]. Самый крупный потребитель серной кислоты — производство минеральных удобрений. На P2O5 фосфорных удобрений расходуется в 2,2—3,4 раза больше по массе серной кислоты, а на (NH4)2SO4 серной кислоты 75 % от массы расходуемого (NH4)2SO4. Поэтому сернокислотные заводы стремятся строить в комплексе с заводами по производству минеральных удобрений.
Токсическое действие





Серная кислота и олеум — очень едкие вещества, поражающие все ткани организма. При вдыхании паров этих веществ они вызывают затруднение дыхания, кашель, нередко — ларингит, трахеит, бронхит и т. д. Попадание кислоты на глаза в высокой концентрации может привести как к конъюнктивиту, так и к полной потере зрения[13].
Предельно допустимая концентрация (ПДК) паров серной кислоты в воздухе рабочей зоны 1 мг/м3, в атмосферном воздухе 0,3 мг/м3 (максимальная разовая) и 0,1 мг/м3 (среднесуточная). Поражающая концентрация паров серной кислоты 0,008 мг/л (экспозиция 60 мин), смертельная 0,18 мг/л (60 мин).
Серная кислота — токсичное вещество. В соответствии с ГОСТ 12.1.007-76 серная кислота является токсичным высокоопасным веществом[14] по воздействию на организм, 2-го класса опасности.
Аэрозоль серной кислоты может образовываться в атмосфере в результате выбросов химических и металлургических производств, содержащих оксиды серы и выпадать в виде кислотных дождей.
В России оборот серной кислоты концентрации 45 % и более — законодательно ограничен[15].
Дополнительные сведения
Мельчайшие капельки серной кислоты могут образовываться в средних и верхних слоях атмосферы в результате реакции водяного пара и вулканического пепла, содержащего большие количества серы. Получившаяся взвесь из-за высокого альбедо облаков серной кислоты, затрудняет доступ солнечных лучей к поверхности планеты. Поэтому (а также в результате большого количества мельчайших частиц вулканического пепла в верхних слоях атмосферы, также затрудняющих доступ солнечному свету к планете) после особо сильных вулканических извержений могут произойти значительные изменения климата. Например, в результате извержения вулкана Ксудач (Полуостров Камчатка, 1907 г.) повышенная концентрация пыли в атмосфере держалась около 2 лет, а характерные серебристые облака серной кислоты наблюдались даже в Париже[16]. Взрыв вулкана Пинатубо в 1991 году, отправивший в атмосферу 3⋅107 тонн серы, привёл к тому, что 1992 и 1993 года были значительно холоднее, чем 1991 и 1994[17].
Стандарты
- Кислота серная техническая ГОСТ 2184—77
- Кислота серная аккумуляторная. Технические условия ГОСТ 667—73
- Кислота серная особой чистоты. Технические условия ГОСТ 14262—78
- Реактивы. Кислота серная. Технические условия ГОСТ 4204—77
Примечания
- ↑ Кислота серная техническая ГОСТ 2184—77
- ↑ name=https://docs.cntd.ru_Серная кислота
- ↑ Ушакова Н. Н., Фигурновский Н. А. Василий Михайлович Севергин: (1765—1826) / Ред. И. И. Шафрановский. М.: Наука, 1981. C. 59.
- ↑ См. также Каменное масло
- ↑ Эпштейн, 1979, с. 40.
- ↑ Эпштейн, 1979, с. 41.
- ↑ Density-Concentration Calculator (англ.). Дата обращения: 21 декабря 2021. Архивировано 21 декабря 2021 года.
- ↑ 8,0 8,1 sulfuric acid hydrogen iodide -> iodine H2S water - Wolfram|Alpha (англ.). www.wolframalpha.com. Дата обращения: 19 мая 2022.
- ↑ 9,0 9,1 9,2 sulfuric acid hydrogen bromide -> bromine sulfur dioxide water - Wolfram|Alpha (англ.). www.wolframalpha.com. Дата обращения: 19 мая 2022.
- ↑ 10,0 10,1 10,2 Ходаков Ю.В., Эпштейн Д.А., Глориозов П.А. § 91. Химические свойства серной кислоты // Неорганическая химия: Учебник для 7—8 классов средней школы. — 18-е изд. — М.: Просвещение, 1987. — С. 209—211. — 240 с. — 1 630 000 экз.
- ↑ Ходаков Ю.В., Эпштейн Д.А., Глориозов П.А. § 92. Качественная реакция на серную кислоту и её соли // Неорганическая химия: Учебник для 7—8 классов средней школы. — 18-е изд. — М.: Просвещение, 1987. — С. 212. — 240 с. — 1 630 000 экз.
- ↑ Sulfuric acid (англ.) // «The Essential Chemical Industry — online»
- ↑ SULFURIC ACID | CAMEO Chemicals | NOAA. cameochemicals.noaa.gov. Дата обращения: 22 мая 2020.
- ↑ name=https://docs.cntd.ru_ГОСТ (недоступная ссылка) 12.1.007-76. ССБТ. Вредные вещества. Классификация и общие требования
- ↑ Постановление Правительства Российской Федерации от 3 июня 2010 года № 398 (недоступная ссылка). Дата обращения: 30 мая 2016. Архивировано 30 июня 2016 года.
- ↑ см. статью «Вулканы и климат» Архивная копия от 28 сентября 2007 на Wayback Machine (рус.)
- ↑ Русский архипелаг — Виновато ли человечество в глобальном изменении климата? Архивная копия от 1 декабря 2007 на Wayback Machine (рус.)
Литература
- Справочник сернокислотчика [Текст] / А. С. Ленский, П. А. Семенов, Г. А. Максудов; ред. К. М. Малин. — 2 изд., перераб. и доп. — М.: Химия, 1971. — 744 с. — Библиогр. в конце разд.- Предм. указ.: с. 723—744.
- Эпштейн Д. А. Общая химическая технология. — М.: Химия, 1979. — 312 с.
