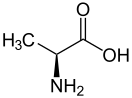
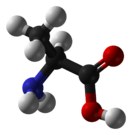
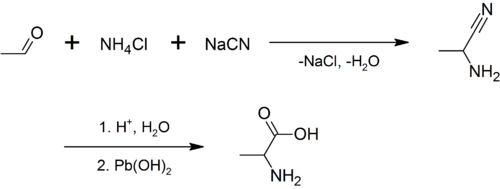Аланин
(перенаправлено с «Ala»)
| Аланин | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
(S)-2-аминопропановая (α-аминопропионовая) кислота | ||
| Сокращения |
Ала, Ala, A GCU,GCC,GCA,GCG |
||
| Хим. формула | NH2-СH(СН3)-СООН | ||
| Рац. формула | C3H7NO2 | ||
| Физические свойства | |||
| Молярная масса | 89,09 г/моль | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 295-316 °C | ||
| Химические свойства | |||
| Константа диссоциации кислоты [math]\displaystyle{ pK_a }[/math] | 2 | ||
| Классификация | |||
| Рег. номер CAS | 56-41-7 | ||
| PubChem | 5950 | ||
| Рег. номер EINECS | 200-273-8 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 16977 | ||
| ChemSpider | 5735 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Алани́н (2-аминопропановая кислота) — алифатическая аминокислота. α-Аланин входит в состав многих белков, β-аланин — в состав ряда биологически активных соединений.
Аланин легко превращается в печени в глюкозу. Этот процесс носит название глюкозо-аланинового цикла и является одним из основных путей глюконеогенеза в печени.
Химические свойства
- взаимодействие с основаниями:
- [math]\displaystyle{ \mathsf{CH_3\text{-}CH(NH_2)\text{-}COOH + NaOH \rightarrow CH_3\text{-}CH(NH_2)\text{-}COONa + H_2O} }[/math]
- взаимодействие с кислотами:
- [math]\displaystyle{ \mathsf{CH_3\text{-}CH(NH_2)\text{-}COOH + HCl \rightarrow [CH_3\text{-}CH(NH_3)\text{-}COOH]^+Cl^-} }[/math]
- взаимодействие со спиртами (реакция этерификации):
- [math]\displaystyle{ \mathsf{CH_3\text{-}CH(NH_2)\text{-}COOH + CH_3OH \rightarrow CH_3\text{-}CH(NH_2)\text{-}COO\text{-}CH_3 + H_2O} }[/math]
- образование пептидной связи:
- [math]\displaystyle{ \mathsf{CH_3\text{-}CH(NH_2)\text{-}COOH + CH_3\text{-}CH(NH_2)\text{-}COOH \rightarrow CH_3\text{-}CH(NH_2)\text{-}CO\text{-}NH\text{-}CH(CH_3)\text{-}COOH + H_2O} }[/math]
Синтез
Впервые аланин был синтезирован Штреккером в 1850 г. действием на ацетальдегид аммиаком и синильной кислотой с последующим гидролизом образовавшегося α-аминонитрила[1]:
В лабораторных условиях аланин синтезируют взаимодействием с аммиаком α-хлор или α-бромпропионовой кислоты[2]:
Примечания
- ↑ Strecker, Ann. 75, 29 (1850).
- ↑ Kendall, E. C.; McKenzie, B. F. Organic Syntheses, Coll. Vol. 1, p.21 (1941); Vol. 9, p.4 (1929) (англ.). Дата обращения: 31 декабря 2014. Архивировано 27 ноября 2015 года.
Литература
- Нечаев А. П. Органическая химия / Нечаев А. П., Еременко Т. В.. — М.: Высшая школа, 1985. — 463с.
- Петров А. А. Органическая химия: Учебник для химико-технологических вузов и факультетов / Петров А. А., Бальян Х. В.,
- Терещенко А. Т. Органическая химия [Учебник для хим.-технол. вузов и фак.] // Под редакцией А. А. Петрова. — 4-е изд. — М: Высшая школа, 1981. — 592 с.
- Степаненко Б. Н. Курс органической химии: Учебник для мед. институтов. — 3-е изд. — М: Медицина, 1979. — 432 с.
- Тейлор Г. Основы органической химии. — М.: Мир, 1989. — 384 с.