Ди-трет-бутилдикарбонат
Ди-трет-бутилдикарбонат — реагент, широко используемый в органическом синтезе для защиты аминогрупп и получения Boc-производных аминов. Представляет собой бесцветную жидкость с характерным резким запахом.
Получение
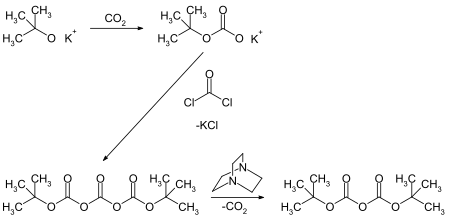
Ди-трет-бутилдикарбонат получают действием фосгена на трет-бутилкарбонат калия с последующим разложением полученного ди-трет-бутилтрикарбоната под действием основных катализаторов, например, 1,4-диаза[2.2.2]октана[1].
Физические свойства
Ди-трет-бутилдикарбонат хорошо растворим в большинстве органических растворителей (декалин, толуол, четырёххлористый углерод, тетрагидрофуран, диоксан, спирты, ацетон, ацетонитрил, диметилформамид), но нерастворим в холодной воде[1].
Применение в органическом синтезе
Ди-трет-бутилдикарбонат широко применяется для введения трет-бутоксикарбонильной (Boc) защитной группы в амины. Данная группа может быть удалена в кислой среде (обычно проводят удаление трифторуксусной кислотой) либо при нагревании. Данная защитная группа устойчива в основной среде и не подвержена действию многих нуклеофилов. Такая стратегия защиты нашла применение не только в синтезе пептидов, но и была расширена на синтез углеводов и алкалоидов[1].
Ди-трет-бутилдикарбонат быстро реагирует с аминами в органических растворителях, давая Boc-производные. При этом в качестве побочных продуктов образуются лишь трет-бутиловый спирт и диоксид углерода, которые легко удаляются при упаривании растворителя. Алифатические и ароматические амины удавалось защищать в различных условиях. Анилины иногда необходимо кипятить с реагентом в тетрагидрофуране, чтобы получить искомый продукт с хорошим выходом[1].
В щелочной среде ди-трет-бутилдикарбонат реагирует с фенолами, давая Boc-производные по гидроксильной группе. В присутствии катализатора межфазного переноса удаётся защищать также спирты, енолы и тиолы. В присутствии DMAP с ди-трет-бутилдикарбонатом реагируют даже амиды и лактамы, обладающие слабыми нуклеофильными свойствами[1].
Ди-трет-бутилдикарбонат может использоваться и для активации карбоксильной группы. В присутствии пиридина он образует смешанные ангидриды с карбоновыми кислотами, которые могут реагировать с ещё одним эквивалентом карбоновой кислоты, давая симметричные ангидриды, либо с другими нуклеофилами. При этом важно, чтобы смешанный ангидрид реагировал с нуклеофилом быстрее, чем сам ди-трет-бутилдикарбонат[1].
Хранение и использование
Реагент следует хранить в холодильнике и не допускать контакта с влагой. Также ди-трет-бутилдикарбонат нельзя нагревать выше 80 °С. Вещество огнеопасно[1].
Примечания
Ссылки
- Sigma-Aldrich. ИК-спектр ди-трет-бутилдикарбоната. Дата обращения: 3 января 2015. Архивировано 24 сентября 2015 года.
- Sigma-Aldrich. КР-спектр ди-трет-бутилдикарбоната. Дата обращения: 3 января 2015. Архивировано 8 января 2015 года.
- Sigma-Aldrich. ЯМР-спектр ди-трет-бутилдикарбоната. Дата обращения: 3 января 2015. Архивировано 24 сентября 2015 года.