Пирофосфат кальция
| Пирофосфат кальция | |
|---|---|
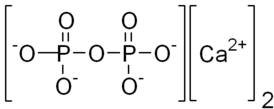 | |
| Общие | |
| Систематическое наименование |
Пирофосфат кальция |
| Традиционные названия | Фосфорнокислый (пиро) кальций |
| Хим. формула | Ca2P2O7 |
| Физические свойства | |
| Состояние | Белые кристаллы |
| Молярная масса | 254,10 г/моль |
| Плотность | 3,09 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1230; 1350 °C |
| Оптические свойства | |
| Показатель преломления | 1,60 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Пирофосфат кальция — неорганическое соединение, соль кальция и пирофосфорной кислоты с формулой Ca2P2O7. Образует кристаллогидрат.
Получение
- Разложением гидроортофосфата кальция:
- [math]\displaystyle{ \mathsf{ 2\ CaHPO_4 \ \xrightarrow{\gt 100^oC}\ Ca_2P_2O_7 + H_2O } }[/math]
- Обменной реакцией с пирофосфатом натрия:
- [math]\displaystyle{ \mathsf{Na_4P_2O_7 + 2\ CaCl_2 \ \xrightarrow{\ }\ Ca_2P_2O_7 + 4\ NaCl } }[/math]
Физические свойства
Безводный пирофосфат кальция образует белые кристаллы, нерастворимые в воде.
Известен кристаллогидрат Ca2P2O7•5H2O, бесцветные кристаллы с плотностью 2,25 г/см³.
Химические свойства
- Пирофосфат кальция гидролизуется в перегретых парах воды:
- [math]\displaystyle{ \mathsf{ 3\ Ca_2P_2O_7 + 3\ H_2O \ \xrightarrow{280^oC}\ 2\ Ca_3(PO_4)_2 + 2\ H_3PO_4 } }[/math]
Применение
Применяется в качестве мягкого абразива в составе зубных порошков, как компонент жидких моющих средств, зубных цементов.
Литература
- Ксензенко В. И., Стасиневич Д. С. Кальция фосфаты // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1990. — Т. 2: Даффа—Меди. — С. 299. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1971. — Т. 1. — 561 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.