Иодоформ
| Иодоформ | |
|---|---|
  | |
 | |
| Общие | |
| Систематическое наименование |
Иодоформ |
| Хим. формула | СНІ3 |
| Физические свойства | |
| Состояние | жёлтые кристаллы |
| Молярная масса | 393.73 г/моль |
| Плотность | 4.008 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 123 °C |
| • кипения | 217 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 0.1 г/л |
| Структура | |
| Координационная геометрия | тетрагональная |
| Кристаллическая структура | гексагональная |
| Классификация | |
| Рег. номер CAS | [75-47-8] |
| Безопасность | |
| ЛД50 | мг/кг |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |

Иодоформ (трииодметан) — органическое соединение с химической формулой СНІ3, имеет вид жёлтых кристаллов с сильным характерным запахом.
Описание
Иодоформ представляет собой жёлтые кристаллы, практически нерастворимые в воде. Трудно растворимы в спирте, хорошо растворяются в эфире, хлороформе.
Получение
Иодоформ получают из этанола, изопропанола или ацетона, действием иода и щелочей, аммиака или карбонатов щелочных металлов:
- [math]\displaystyle{ \mathsf{6NaHCO_3 + 4I_2 + C_2H_5OH \rightarrow CHI_3\downarrow + HCOONa + 5NaI + 5H_2O + 6CO_2\uparrow} }[/math]
Реакция протекает по следующей схеме:
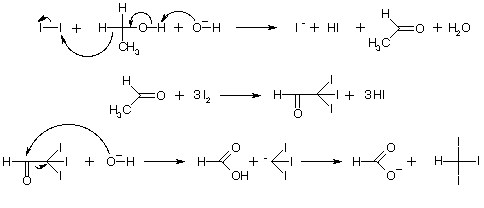
Иодоформ также можно получить электролизом иодида калия или натрия в спиртовом растворе. При электролизе образуются иод и щёлочь, необходимые для процесса. Образующийся при реакции иодид калия (натрия) снова подвергается электролизу, и таким образом весь иод соли идёт на образование иодоформа.
Также иодоформ можно получить йодоформной пробой.
Биологические свойства
Умеренно-ядовит.
Применение
- В медицине иодоформ применяют как антисептик. В частности, используется для полоскания горла.
- В стоматологии в ряде случаев, йодоформ применяют для тампонады лунки после удаления зуба.
