Дигидроксид-оксид титана
| Дигидроксид-оксид титана | |
|---|---|
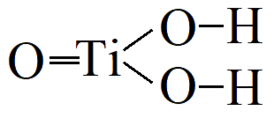 | |
| Общие | |
| Систематическое наименование |
Дигидроксид-оксид титана |
| Традиционные названия | Метатитановая кислота, β-титановая кислота |
| Хим. формула | TiO(OH)2 |
| Физические свойства | |
| Состояние | белое аморфное вещество |
| Молярная масса | 97,89 г/моль |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Дигидрокси́д-окси́д тита́на (метатитановая кислота, β-титановая кислота) — неорганическое соединение, оксогидроксид титана с формулой TiO(OH)2 или H2TiO3, белое аморфное вещество, не растворимое в воде.
Получение
- Действие раствора щелочи на растворимую оксосоль титана:
- [math]\displaystyle{ \mathsf{TiOSO_4 + 2NaOH \ \xrightarrow{}\ TiO(OH)_2\downarrow + Na_2SO_4 } }[/math]
- Действие раствора щелочи на растворимую соль титана(IV):
- [math]\displaystyle{ \mathsf{TiCl_4 + 4NaOH \ \xrightarrow{}\ TiO(OH)_2\downarrow + 4NaCl + H_2O } }[/math]
- Возникает при медленном распаде ортотитановой кислоты:
- [math]\displaystyle{ \mathsf{H_4TiO_4 \ \xrightarrow{}\ H_2TiO_3 + H_2O } }[/math]
Физические свойства
Дигидроксид-оксид титана — белое аморфное вещество.
Из раствора выпадает в виде гидрата TiO2·n H2O. Свежеосаждённое вещество химически активнее «старого» осадка.
Химические свойства
- Разлагается при нагревании:
- [math]\displaystyle{ \mathsf{TiO(OH)_2 \ \xrightarrow{600-700^oC}\ TiO_2 + H_2O } }[/math]
- Реагирует с концентрированными кислотами:
- [math]\displaystyle{ \mathsf{TiO(OH)_2 + H_2SO_4 \ \xrightarrow{100^oC}\ TiOSO_4\downarrow + 2H_2O } }[/math]
- [math]\displaystyle{ \mathsf{TiO(OH)_2 + 2HNO_3 \ \xrightarrow{}\ Ti(NO_3)_2(OH)_2 + H_2O } }[/math]
- Реагирует с перекисью водорода (качественное обнаружение):
- [math]\displaystyle{ \mathsf{TiO(OH)_2 + H_2O_2 + (n-2)H_2O \ \xrightarrow{}\ TiO(O_2)\cdot n H_2O\downarrow } }[/math] — жёлтый осадок;
- [math]\displaystyle{ \mathsf{TiO(OH)_2 + H_2O_2 + 2HNO_3 + H_2O \ \xrightarrow{}\ [Ti(H_2O)_4](O_2)(NO_3)_2\downarrow } }[/math] — жёлтый осадок;
- [math]\displaystyle{ \mathsf{TiO(OH)_2 + H_2O_2 + 4KOH \ \xrightarrow{}\ K_4[Ti(O_2)_4]\downarrow + 7H_2O } }[/math] — бесцветный раствор.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-82270-092-4.
- Справочник химика / Редкол.: Никольский Б. П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р. А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.