Гидрид калия
| Гидрид калия | |
|---|---|
 K+ H− K+ H− | |
| Общие | |
| Систематическое наименование |
калия гидрид |
| Хим. формула | KH |
| Рац. формула | HK |
| Физические свойства | |
| Состояние | белое твердое вещество |
| Молярная масса | 40.1062 г/моль |
| Плотность | 1.47 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 400 °C |
| Мол. теплоёмк. | 37,91 Дж/(моль·К) |
| Энтальпия | |
| • образования | -57,82 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в веществах |
бензол: не растворим вода: реагирует диэтиловый эфир: не растворим сероуглерод: не растворим этанол: реагирует[1] |
| Структура | |
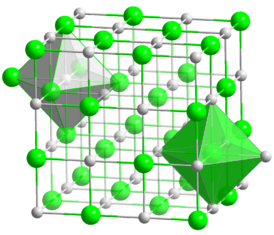
| Кристаллическая структура | кубическая, пространственная группа Fm3m |
| Классификация | |
| Рег. номер CAS | 7693-26-7 |
| Безопасность | |
| Пиктограммы ECB |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидрид калия — это неорганическое бинарное химическое соединение белого цвета. Химическая формула KH.
Физические свойства
Гидрид калия образует бесцветные ионные кристаллы кубической сингонии с решеткой типа NaCl (a = 0.57 нм). Хорошо растворим в расплавленном калии, не растворяется в органических растворителях. Обладает высокой теплопроводностью.
Химические свойства
Гидрид калия является ионным соединением K+H−. Его расплав проводит электрический ток, при электролизе на аноде выделяется водород.
Вещество нестабильно и при нагревании распадается на компоненты:
- [math]\displaystyle{ \mathsf{2KH \xrightarrow{400^oC, vacuum} \ 2K+H_2 } }[/math]
Гидрид калия обладает высокой химической активностью, является сильным восстановителем. Окисляется кислородом:
- [math]\displaystyle{ \mathsf{2KH + O_2 \xrightarrow{200^oC} \ 2KOH } }[/math]
Взаимодействует с водой:
- [math]\displaystyle{ \mathsf{KH + H_2O \ \xrightarrow{} \ KOH + H_2\uparrow } }[/math]
- [math]\displaystyle{ \mathsf{KH + HCl \ \xrightarrow{} \ KCl + H_2\uparrow } }[/math]
- [math]\displaystyle{ \mathsf{KH + HO-R \ \xrightarrow{} \ KOR + H_2\uparrow } }[/math]
и газообразным аммиаком:
- [math]\displaystyle{ \mathsf{KH + NH_3 \xrightarrow{300^oC} \ KNH_2 + H_2\uparrow } }[/math]
Взаимодействует с галогенами:
- [math]\displaystyle{ \mathsf{KH + Cl_2 \xrightarrow{400^oC} \ KCl + HCl\uparrow } }[/math]
С углекислотой образует формиат калия:
- [math]\displaystyle{ \mathsf{KH + CO_2 \xrightarrow{150^oC, \mathit{p}} \ K(HCOO) } }[/math]
Взаимодействует с оксидом кремния:
- [math]\displaystyle{ \mathsf{4KH + 3SiO_2 \xrightarrow{500^oC} \ 2K_2SiO_3 + Si + 2H_2 } }[/math]
Получение
Гидрид калия получают прямой реакцией расплавленного калия с водородом под давлением:
- [math]\displaystyle{ \mathsf{2K+H_2 \xrightarrow{200-350^oC, \mathit{p}} \ 2KH} }[/math]
Эта реакция была открыта Гемфри Дэви вскоре после его открытия в 1807 году калия, когда он отметил, что металл будет испаряться в токе водорода при нагревании только ниже точки кипения.
Токсичность
Едкое вещество, разъедает органические вещества. Огнеопасно.
См. также
Примечания
- ↑ [www.xumuk.ru/spravochnik/507.html Сайт XuMuK.ru]. Дата обращения: 30 марта 2010.