Нейраминидаза
Нейраминида́за (КФ 3.2.1.18) — фермент, относящийся к гликозил-гидролазам. Номенклатурное название — экзо-α-сиалидаза. Также употребимы названия: α-нейраминидаза, N-ацилнейраминидатгликогидролаза, сиалидаза. Катализируемые реакции: гидролиз α-2→3-, α-2→6-, α-2→8-кетозидных связей концевых остатков сиаловой кислоты в олигосахаридах, гликопротеинах, гликолипидах и синтетических соединениях.
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Разнообразие нейраминидаз
Нейраминидаза широко распространена в природе, она входит в состав оболочек некоторых вирусов. Обнаружена в ряде патогенных микроорганизмов (впервые была открыта в культуре возбудителей газовой гангрены Clostridium perfringens), a также у позвоночных и беспозвоночных животных. У растений нейраминидаза не обнаружена.
Фермент строго специфичен по отношению к конфигурации кетозидной связи и относительно специфичен к положению этой связи в молекуле. Нейраминидаза из холерного вибриона и возбудителя газовой гангрены, обычно применяющиеся в лабораторной практике, могут расщеплять α-2→3- и α-2→6-кетозидные связи. Вирусные нейраминидазы, как правило, обладают более строгой специфичностью по отношению к положению α-кетозидной связи. Фермент не требует кофакторов, но некоторые из нейраминидаз активируются ионами Са2+.
К настоящему времени ферменты с сиалидазной активностью входят в состав 3-х семейств гликозил-гидролаз: GH33, GH34, GH83.[1] Для всех трех семейств характерна структура 6-лопастного-β-пропеллера. В семейство GH33 включены ферменты, обнаруженные у бактерий, различных эукариот и вирусов. Для них также характерно наличие транссиалидазной активности КФ 2.4.1.-.[2] К семейству GH34 принадлежат молекулы вирусного происхождения.[3] В семейство GH83 входят вирусные гемагглютинин-нейраминидазы.[4]
Является одним из двух основных поверхностных антигенов вируса гриппа. Указание типа нейраминидазы используется в обозначении подтипа вируса: например, H5N1 (буква H от «гемагглютинин»).
Нейраминидаза вируса гриппа
Открытие
Существование ферментативной активности на поверхности вириона вируса гриппа было открыто американским вирусологом Джорджем Кеблом Хёрстом (George Keble Hirst, 02.03.1909—22.01.1994) в 1942 году. Он инкубировал эритроциты с вирусом, наблюдая за реакцией гемагглютинации, и отметил, что агглютинация не является устойчивой[5].
Биологическая роль
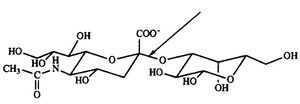
Как известно на сегодняшний день, один из поверхностных гликопротеинов вириона гриппа, гемагглютинин, прикрепляется к полисахаридным цепочкам на поверхности эритроцитов, содержащим остатки сиаловой кислоты. Другой поверхностный гликопротеин, нейраминидаза, специфически отщепляет остаток сиаловой (N-ацетилнейраминовой) кислоты от полисахаридов мембраны эритроцита, тем самым разрушая рецепторы к вирусу на клетках организма-хозяина. Нейраминидаза разрушает α-кето-связь между концевой N-ацетилнейраминовой кислотой и соседним углеводным остатком, обычно, галактозой. Вирусный фермент демонстрирует некоторое «предпочтение» α-2→3 связям[6].
Роль фермента, разрушающего рецепторы к вирусу, не ясна до конца. Предполагается, что активность нейраминидазы помогает вирусным частицам проникать через секреты слизистых, богатых сиаловой кислотой, для достижения вирионами клеток-мишеней эпителия дыхательных путей[7]. Также экспериментально подтверждена роль фермента в облегчении высвобождения вновь образованных вирусных частиц с поверхности заражённых клеток, где те могут агрегироваться в результате взаимодействия вирусного гемагглютинина с сиаловой кислотой на мембране клетки[8].
Антигенная специфичность
Как и гемагглютинин, нейраминидаза — очень важный поверхностный антиген вируса. Для вируса гриппа типа А обнаружено две антигенные вариации. Изменения в аминокислотной последовательности антигенов идут постоянно из-за давления отбора антител иммунизированной популяции. В результате генетической рекомбинации появляются вирусы с антигенной последовательностью, значительно (до 50 %) отличающейся от таковой у циркулирующих штаммов. Такие изменения в подтипах как по гемагглютинину, так и нейраминидазе произошли у человеческого гриппа в 1957 году (когда вирус H1N1 перешёл в H2N2), в 1968 (H2N2 в H3N2) и в 1977 (H3N2 в H1N1, хотя вирус H3N2 продолжил циркулировать)[9]. Подобные мутации ответственны за большинство пандемий, прошедших в последнее время. Различия между подтипами выявляются по отрицательной перекрестной реакции на сыворотку к каждому из них. Вирус гриппа типа B не выявляет подобной смены антигенной специфичности, хотя изменения в строении антигенов также происходят.
Антитела к нейраминидазе снижают тяжесть заболевания [10], но не приводят к излечению от инфекции, что согласуется с ролью нейраминидазы в жизненном цикле вируса.
Структура
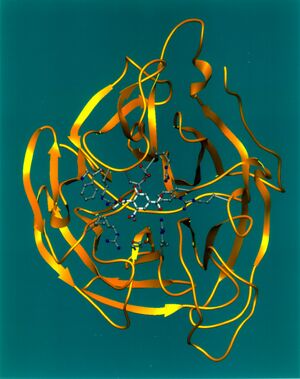
Нейраминидаза — это тетрамер, заякоренный в вирусной мембране с помощью одной гидрофобной последовательности из 29 аминокислот, расположенной возле N-конца белка. Из разрушенной вирусной мембраны выделяется белок с молекулярной массой 200 кДа, содержащий 4 идентичные гликозилированные субъединицы, который обладает всеми антигенными и ферментативными свойствами мембрансвязанной нейраминидазы[11]. Этот белок был кристаллизован и его структура изучена с помощью УФ-дифракции.
Схематично структуру нейраминидазы можно представить как 6 4-цепочечных антипараллельных β-слоя, расположенных как лопасти пропеллера.[12] Центральная (первая) цепь каждого слоя параллельна оси пропеллера, остальные же располагаются практически перпендикулярно относительно неё. Крайняя цепь первого слоя соединена с центральной цепью слоя, следующего за ним. Это соединение расположено на поверхности молекулы фермента и несет множество антигенно и энзиматически важных аминокислот.[13][14][15]
Четыре одинаковых субъединицы расположены радиально. Активный центр фермента расположен по центру каждой из субъединиц. Он представляет собой глубокий карман, окруженный стенками, аминокислотная последовательность которых инвариантна для всех известных штаммов вируса. Эти аминокислоты активного центра можно разделить на 2 типа: одни участвуют в непосредственном контакте с субстратом, другие же выполняют лишь функцию поддержания структуры.[16]
С помощью кристаллографии определено наличие олигосахаридных цепочек, прикрепленных к протеину и имеющих вид антенн.[9]
Ингибиторы нейраминидазы гриппа
Поиск ингибиторов нейраминидазы гриппа начался в 1966 году [17]. Поводом для этого послужило предположение, что подобные вещества будут проявлять противовирусную активность.
Первый ингибитор, диен α-сиаловой кислоты (Neu5Ac2en), был синтезирован в 1969 году[18]. Множество аналогов вещества Neu5Ac2en было синтезировано в 70-е годы XX столетия, наиболее сильным ингибитором оказалось трифторацетил-производное Neu5Ac2en. Данное вещество использовалось для изучения роли нейраминидазы в жизненном цикле вируса, но противовирусной его активности обнаружено не было.[19]
Ингибитором нейраминидазы является широко известный противовирусный препарат Осельтамивир.
См. также
Литература
- ↑ CAZy — GH. Дата обращения: 2 апреля 2007. Архивировано 27 сентября 2013 года.
- ↑ CAZy — GH33. Дата обращения: 2 апреля 2007. Архивировано 25 февраля 2007 года.
- ↑ CAZy — GH34. Дата обращения: 2 апреля 2007. Архивировано 16 августа 2007 года.
- ↑ CAZy — GH83. Дата обращения: 2 апреля 2007. Архивировано 20 июля 2007 года.
- ↑ Hirst, G. K. Adsorption of influenza haemagglutinins and virus by redblood cells : [англ.] // Journal of Experimental Medicine. — 1942. — Vol. 76, no. 2 (August). — P. 195–209. — doi:10.1084/jem.76.2.195. — PMID 19871229. — PMC 2135226.
- ↑ Corfield A.P., Wember M., Schauer R., Rott R. The specificity of viral sialidases. The use of oligosaccharide substrates to probee nzyme characteristics and strain specific differences. // Eur JBiochem 124, 1982, 521—525.
- ↑ Allen A. Mucus — A protective secretion of complexity. // Trends Biochem Sci, 1983, 169—173.
- ↑ Palese P., Tobita K., Ueda M., Compans R.W. Characterisation of temperature sensitive influenza virus mutants defective in neuraminidase. // Virology 61, 1974, 397—410.
- ↑ Перейти обратно: 9,0 9,1 Colman P.M. Influenza virus neuraminidase: Structure, antibodies, and inhibitors. // Protein Science. — 1994. — 3:1687-1696. Cambridge University Press.
- ↑ Kilbourne E.D., Laver W.G., Schulman J.L., Webster R.G. Antiviral activity of antiserum specific for an influenza virus neuraminidase. // J Virol 2, 1968, 281—288.
- ↑ Laver W.G. Crystallisation and peptide maps of neuraminidase heads from H2N2 and H3N2 influenza virus strains. // Virology 86, 1978, 87.
- ↑ Varghese J.N., Laver W.G., Colman P.M. Structure of the influenza virus glycoprotein antigen neuraminidase at 2.9 Å resolution. // Nature. — 1983. — 303: 35-40.
- ↑ Colman P.M., Varghese J.N., Laver W.G. Structure of the catalytic and antigenic sites in influenza virus neuraminidase. // Nature. — 1983. — 303:41-44.
- ↑ Varghese J.N., Colman P.M. Three-dimensional structure of the neuraminidase of influenza virus A/Tokyo/3/67 at 2.2 Å resolution. // JMol Biol221. — 1991. — p. 473—486.
- ↑ Varghese J.N., McKimm-Breschkin J., Caldwell J.B., Kortt A.A., Colman P.M. The structure of the complex between influenza virus neuraminidase and sialic acid, the viral receptor. Proteins Struct Funct Genetics. — 1992. — 14:327-332.
- ↑ Colman P.M., Hoyne P.A., Lawrence M.C. Sequence and structure alignment of paramyxovirus haemagglutinin-neuraminidase (HN) with influenza virus neuraminidase. // J Virol. — 1993. — 67:2972-2980.
- ↑ Edmond J.D., Johnston R.G., Kidd D., Rylance H.J., Sommerville R.G. The inhibition of neuraminidase and antiviral action. // Br J Pharmacol Chemother. — 1966. — 27, p. 415—426.
- ↑ Meindl P., Tuppy H. 2-Deoxy-2,3-dehydrosialica cids. I. Synthesis and properties of 2-deoxy-2,3-dehydro-N-acylneuraminic acids and their methyl esters. // Monatsh Chem. — 1969. — 100, p. 1295—1306.
- ↑ Palese P., Schulman J.L. Inhibitors of viral neuraminidase as potential antiviral drugs. In: Oxford JS, ed. Chemoprophylaxis and virus infections of the upper respiratory tract. — 1977. — vol I . Boca Raton, Florida: CRC Press. p. 189—205.