Ацетат кальция
| Ацетат кальция | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
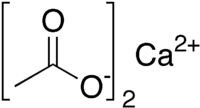
Ацетат кальция |
| Сокращения | Ca(OAc)2 |
| Традиционные названия | Пригорело-древесная соль[1] |
| Хим. формула | Ca(CH3COO)2 |
| Рац. формула | CaC4H6O4 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 158.138 г/моль |
| Плотность | 1.6 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 160 (с разложением)[2] |
| Химические свойства | |
| Растворимость | |
| • в воде | 40 г/100 мл |
| Классификация | |
| Рег. номер CAS | 62-54-4 |
| SMILES | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетат кальция — кальциевая соль уксусной кислоты. Бесцветное кристаллическое или аморфное вещество, хорошо растворимое в воде. Технический моногидрат может быть в форме гранул или некрупных игл. Обладает слабым вкусом и запахом уксуса. Химическая формула — Ca(CH3COO)2, однако чаще получают его моногидрат Ca(CH3COO)2•H2O.[3]
История названия
Пригорело-древесная соль — старинное название ацетата кальция — в старину получалась при сухой перегонке древесины, из-за чего древесина, естественно, обугливалась, «пригорала». Из-за того, что метод сухой перегонки древесины использовался алхимиками с незапамятных времён[4], установить человека, давшего такое название этой соли или впервые получившего её, невозможно.
Получение
В лаборатории получают действием уксусной кислоты на карбонат, оксид или гидроксид кальция.[5]
- [math]\displaystyle{ \mathsf{2CH_3COOH + CaCO_3 \rightarrow Ca(CH_3COO)_2 + H_2O + CO_2 \uparrow} }[/math]
- [math]\displaystyle{ \mathsf{2CH_3COOH + CaO \rightarrow Ca(CH_3COO)_2 + H_2O } }[/math]
- [math]\displaystyle{ \mathsf{2CH_3COOH + Ca(OH)_2 \rightarrow Ca(CH_3COO)_2 + 2H_2O} }[/math]
- Также возможно получение из простого вещества:
- [math]\displaystyle{ \mathsf{2CH_3COOH + Ca \rightarrow Ca(CH_3COO)_2 + H_2\uparrow} }[/math]
Применение
Не имеет промышленного применения.
Используется в лаборатории для получения диметилкетона (ацетона). Эту реакцию осуществляют, нагревая ацетат кальция до 160 °С[2][6]:
- [math]\displaystyle{ \mathsf{Ca(CH_3COO)_2 \xrightarrow{160^\circ C} CaCO_3 + (CH_3)_2CO} }[/math]
Именно из-за этой реакции ацетат кальция нельзя хранить или сушить вблизи открытого огня, а помещения, в которых происходят работы с ацетатом кальция, должны быть оборудованы приточно-вытяжной вентиляцией.[7]
Также может применяться в лаборатории для получения сложных эфиров уксусной кислоты — алкилацетатов:
- [math]\displaystyle{ \mathsf{Ca(CH_3COO)_2 + 2CH_3CH_2Br \rightarrow CaBr_2 + 2CH_3COOCH_2CH_3} }[/math]
Также ацетат кальция используется для получения ацетата калия обменными реакциями из карбоната и/или бикарбоната калия:
- [math]\displaystyle{ \mathsf{Ca(CH_3COO)_2 + 2KHCO_3\rightarrow 2CH_3COOK + Ca(HCO_3)_2} }[/math]
- [math]\displaystyle{ \mathsf{Ca(CH_3COO)_2 + K_2CO_3\rightarrow 2CH_3COOK + CaCO_3} }[/math]
Также ацетат кальция применяют при получении лавсана в качестве катализатора.[3]
Ещё одним способом применения ацетата кальция является приготовление аналога сухого спирта — твёрдого спиртового сольвата ацетата кальция — при смешивании ацетата кальция и этилового спирта.
Пищевая промышленность
Ацетат кальция зарегистрирован в пищевой промышленности в качестве пищевой добавки группы консервантов E263.[8] Может применяться как консервант, регулятор кислотности, уплотнитель растительных тканей. Останавливает развитие болезнетворных бактерий в хлебобулочных изделиях, смягчает ярко выраженный кислый вкус консервированных овощей и фруктов. В сельскохозяйственной промышленности используется для консервации кормов.[9] Так как действие ацетата кальция ограничено наличием в продуктах сульфатов, фосфатов, карбонатов и гидрокарбонатов, которые в конечном итоге дают осадки с катионом [math]\displaystyle{ \mathsf{Ca^{2+}} }[/math], то применять его лучше в сочетании с другими консервантами.
| Массовая доля основного вещества,безводная форма, %, не менее | 98 |
| Потери при просушке, %, не более | 11 |
| pH 10%-го водного раствора | 6-9 (включительно) |
| Массовая доля нерастворимых веществ, %, не более | 0,3 |
Медицина
Ацетат кальция оказывает абсорбирующее действие на анионы фосфорных кислот:
- [math]\displaystyle{ \mathsf{3Ca(CH_3COO)_2 + 2PO_4^{3-}\rightarrow 6CH_3COO^- + Ca_3(PO_4)_2\downarrow} }[/math]
Также ацетат кальция восстанавливает положительный кальциевый баланс у больных с почечной недостаточностью в легкой, средней и тяжелой форме и у больных, находящихся на гемодиализе или перитонеальном диализе[10]. Является безалюминиевым и безмагниевым фосфат-связывающим препаратом (фосфат-биндером). Фосфат-связывающая способность ацетата кальция в 2 раза выше, а всасываемость его в кишечнике значительно меньше, чем у кальция карбоната.
Примечания
- ↑ ТРИВИАЛЬНЫЕ НАЗВАНИЯ ВЕЩЕСТВ. Дата обращения: 29 мая 2013. Архивировано 28 января 2012 года.
- ↑ 2,0 2,1 Ацетат кальция е263 (e263) | Пищевые добавки «НОРД». Архивировано 5 июня 2013 года.
- ↑ 3,0 3,1 Кальций уксуснокислый Химическая формула: Ca(CH3COO)2*H2O Синоним: Ацетат кальция, кальциевая соль уксусной кислоты, кальций ацетат Международное название: Сalcium acetate ||О … (недоступная ссылка). Дата обращения: 29 мая 2013. Архивировано 12 декабря 2013 года.
- ↑ И. Я. Миттова, А. М. Самойлов, История химии с древнейших времен до конца XX века//М.: Химия, 2012
- ↑ Способ получения ацетата кальция. Патент РФ 2156757. Дата обращения: 1 июня 2013. Архивировано 15 марта 2014 года.
- ↑ СаОН вместо NaОН. Дата обращения: 5 мая 2020. Архивировано 14 сентября 2017 года.
- ↑ ГОСТ Р 54537-2011
- ↑ E263 — Ацетат кальция (Е263). Архивировано 5 июня 2013 года.
- ↑ Консервант Е263 (Ацетат кальция) » Пищевые добавки. Дата обращения: 30 мая 2013. Архивировано 7 августа 2013 года.
- ↑ Нефродин. Ацетат кальция — Аннотация. Архивировано 5 июня 2013 года.