Хромотроповая кислота
| Хромотроповая кислота | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
4,5-дигидрокси-2,7-нафталиндисульфоновая кислота |
| Традиционные названия | Хромотроповая кислота |
| Хим. формула | C10H8O8S2 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 320.29 г/моль |
| Химические свойства | |
| Константа диссоциации кислоты [math]\displaystyle{ pK_a }[/math] | 5.36, 15.6[1] |
| Растворимость | |
| • в воде | растворим |
| • в этаноле | нерастворим |
| • в диэтиловом эфире | нерастворим |
| Классификация | |
| Рег. номер CAS | 148-25-4 |
| SMILES | |
| InChI | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хромотро́повая кислота (4,5-дигидрокси-2,7-нафталиндисульфоновая кислота) — органическое химическое вещество, относящееся к классам сульфокислот и фенолов. Динатриевая соль хромотроповой кислоты (также называемая «хромотроп»), обычно поставляемая в виде дигидрата − реагент в аналитической химии.
Получение
Хромотроповая кислота может быть получена из нафталина сульфированием его до 1,3,6-нафталинтрисульфокислоты, нитрованием последней, восстановлением нитрогруппы до аминогруппы железом в кислой среде и, наконец, нагреванием в автоклаве с 40-50 % водным раствором щелочи, в соответствии со схемой[2]:

Растворы хромотроповой кислоты темнеют при хранении на воздухе. 3,6-Дихлорхромотроповая кислота более устойчива к окислению.[3]
Применение
Определение формальдегида
Хромотроповая кислота используется в качестве селективного реагента для определения формальдегида, реакция с которым в присутствии серной кислоты в концентрации не менее 72 % приводит к образованию красно-фиолетового окрашивания. Предел обнаружения: 0,02 мкг формальдегида.[4] Количественное определение во многих случаях может быть проведено колориметрически. Использование этой реакции позволяет определять формальдегид во многих объектах: тканях, алкогольных напитках[5], почве, сточных водах и т. п. Без изменения объёма пробы можно определить от 0,06 до 1,2 мг формальдегида в 1 л воды. Определению формальдегида в концентрациях от 1 до 10 мг/л мешает фенол (10 мг/л и выше). Ацетальдегид мешает своей окраской только в концентрациях порядка граммов в 1 л. Остальные альдегиды определению не мешают.[6] Точная структура продукта взаимодействия хромотроповой кислоты с формальдегидом неизвестна, в кристаллическом виде он получен не был.[7] Несмотря на то, что в большинстве источников приводится недоказанная структура II, наиболее вероятной в настоящее время считается ксантилиевая структура I.[5]
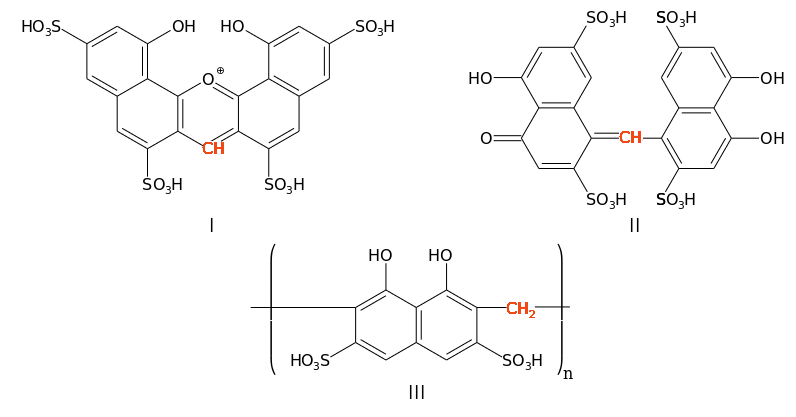
Определение металлов
Натриевая соль хромотроповой кислоты является ценным реагентом в аналитической химии и используется для количественного определения некоторых металлов. Особенно часто рекомендуется как реагент для определения титана (IV), железа (III) и ниобия (V).[8] Так, с Ti (IV) хромотроповая кислота образует водорастворимые коричнево-красные комплексные соединения, состав и окраска которых зависит от кислотности среды, по причине чего определение титана обычно проводят с использованием буферных растворов. Железо (III) мешает определению, поскольку образует с хромотроповой кислотой окрашенные в зелёный цвет комплексные соединения.[3]
Использование в синтезе
Хромотроповая кислота является родоначальником целого ряда важных аналитических реагентов: арсеназо I, арсеназо III, сульфоназо III (Ортаниловый СО), карбоксиарсеназо.[8]
Примечания
- ↑ Dawson, R.M.C. Data for Biochemical Research. — Oxford : Clarendon Press, 1959.
- ↑ Л. Н. Николенко. Лабораторный практикум по промежуточным продуктам и красителям. − М.: Высшая школа, 1965. − С. 138—139.
- ↑ 3,0 3,1 Marczenko Z, Balcerzak M. — Chapter 53. Titanium. — In: Kloczko E. Separation, Preconcentration and Spectrophotometry in Inorganic Analysis — 1st ed. — 2000. eBook ISBN 978-0-08-054108-2
- ↑ Е. В. Сальникова, Е. А. Кудрявцева, С. В. Лебедев, М. Г. Скальная. Токсикологическая химия: учебное пособие. − Оренбург: ОГУ, 2012. − С. 57.
- ↑ 5,0 5,1 (2011) «Formaldehyde in Alcoholic Beverages: Large Chemical Survey Using Purpald Screening Followed by Chromotropic Acid Spectrophotometry with Multivariate Curve Resolution». International Journal of Analytical Chemistry 2011: 11. doi:10.1155/2011/797604.
- ↑ Д. Н. Васкевич, Л. Н. Овсянникова (ред.) Унифицированные методы анализа вод. — М.: Химия, 1971. — С. 327—328
- ↑ (1989) «The chemistry of the chromotropic-acid method for the analysis of formaldehyde». Canadian Journal of Chemistry 67 (5): 871—876. doi:10.1139/v89-135.
- ↑ 8,0 8,1 Л. К. Неудачина, Н. В. Лакиза. Физико-химические основы применения координационных соединений. Учебное пособие. − Екатеринбург: Изд-во Уральского ун-та, 2014. − С. 114.