Тетратионовая кислота
| Тетратионовая кислота | |
|---|---|
 | |
| Общие | |
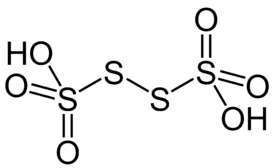
| Хим. формула | H2S4O6 |
| Физические свойства | |
| Молярная масса | 225,873 г/моль |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Тетратионовая кислота H2S4O6 — неорганическая двухосновная кислота. Относится к политионовым кислотам.
Свойства
Тетратионовая кислота является сильной кислотой. Неустойчива, может существовать только в разбавленных водных растворах и разлагается при их концентрировании или нагревании:
- [math]\displaystyle{ \mathsf{H_2S_4O_6 \rightarrow 2S + SO_2 + H_2SO_4} }[/math]
Растворы тетратионовой кислоты в этаноле реагируют с щелочами:
- [math]\displaystyle{ \mathsf{H_2S_4O_6 + 2NaOH \rightarrow Na_2S_4O_6 + 2H_2O} }[/math]
В водных растворах реагирует с щелочами с разложением:
- [math]\displaystyle{ \mathsf{H_2S_4O_6 + 4NaOH \rightarrow 2S + Na_2SO_3 + Na_2SO_4 + 3H_2O} }[/math]
Тетратионовая кислота наряду с другими политионовыми кислотами образуется в реакции Вакенродера при взаимодействии сероводорода и диоксида серы.
Тетратионаты щелочных металлов образуются при окислении соответствующих тиосульфатов иодом:
- [math]\displaystyle{ \mathsf{2Na_2S_2O_3 + I_2 \rightarrow Na_2S_4O_6 + 2NaI} }[/math]
Литература
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.