Теплота парообразования
Энтальпи́я испаре́ния (синоним: теплота́ парообразова́ния) — количество теплоты, которое необходимо сообщить веществу при постоянных давлении и температуре, чтобы перевести его из жидкого состояния в газообразное (в равновесный с жидкостью пар). Энтальпию испарения одного моля вещества называют мольной энтальпией испарения (часто слово «мольная» опускают и говорят просто «энтальпия испарения», подразумевая именно мольную энтальпию).
Единица измерения мольной энтальпии испарения — Дж/моль. Иногда вместо мольной используется удельная энтальпия испарения (Дж/кг).
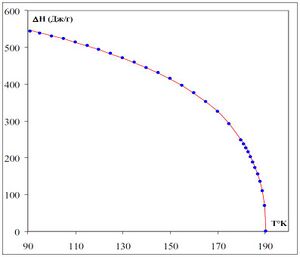
Энтальпия испарения уменьшается с ростом температуры и обращается в ноль в критической точке (см. рисунок).
Зависимость энтальпии испарения от температуры хорошо описывается формулой[1]
- [math]\displaystyle{ \Delta H_v = A\bigl( \rho_f^2-\rho_d^2\bigr)-B\bigl( \rho_f^4-\rho_d^4\bigr), }[/math]
где [math]\displaystyle{ \Delta H_v }[/math] — энтальпия испарения, [math]\displaystyle{ \rho_f }[/math] — плотность жидкости, [math]\displaystyle{ \rho_d }[/math] — плотность пара, находящегося в равновесии с жидкостью, A и В — коэффициенты, связанные с параметрами потенциала Леннард-Джонса.
Литература
- Герасимов Я. И. Курс физической химии. М.: Химия, 1964. Том 1.
- Мелвин-Хьюз Э. А. Физическая химия. М.: Изд-во иностранной литературы, 1962.
Примечания
- ↑ Левинский А. И. Связь плотности жидкости и пара с энтальпией испарения // Журнал физической химии. — 2007. — Т. 80, № 6. — С. 1048—1049.