Нитритометрия
Нитритометрия — метод количественного анализа ароматических аминов, основанный на их титровании нитритом натрия.
Теория
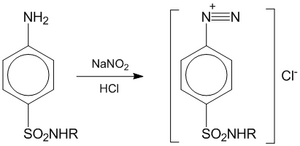
Метод основан на реакции первичных аминов с азотистой кислотой с образованием диазосоединений:
Титрантом является раствор нитрита натрия. Катализатором служит раствор бромида калия, облегчающий процесс диазотирования. Точка эквивалентности определяется при помощи индикаторов — тропеолина 00 (переход от красного цвета раствора к жёлтому), нейтрального красного (переход от красно-фиолетового цвета к синему), иодкрахмальная бумага, а также потенциометрически (с платиновым электродом в качестве индикаторного электрода, хлорсеребряного или каломельного в качестве электрода сравнения). Титрование проводят при пониженной температуре, чтобы избежать разложения азотистой кислоты и соли диазония.
Практика
Для титрования обычно используют 0,1М раствор нитрита натрия. Навеску препарата (например, лекарственного средства класса сульфаниламидов) растворяют в 10 мл воды, прибавляют 10 мл 8,3%-го раствора соляной кислоты, 1 г KBr. Титрование ведут при температуре 15-20°С или 0-5°С до изменения цвета индикатора. Одновременно проводится контрольный опыт.
Нитритометрия используется для количественного анализа соединений с первичной или вторичной ароматической аминогруппой, гидразидов и ароматических нитросоединений после восстановления их нитрогруппы до аминогруппы.
Литература
- Государственная фармакопея Российской Федерации, выпуск XII
- В. Г. Беликов. Фармацевтическая химия. Ч.2. — Пятигорск, 1996. — 608 с. — 5000 экз. — ISBN 5-06-003253-1.