Оксид фосфора(V)
| Оксид фосфора(V) | |
|---|---|
  | |
 | |
| Общие | |
| Систематическое наименование |
Оксид фосфора(V) |
| Традиционные названия | Фосфорный ангидрид; пентаоксид фосфора |
| Хим. формула | P2O5 |
| Рац. формула | P2O5 |
| Физические свойства | |
| Состояние | белый порошок |
| Молярная масса | 141,94 г/моль |
| Плотность | 2.39 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 420оС(Н-форма),569 (О-форма) |
| • кипения | возгоняется при 359 (Н-форма) °C |
| Энтальпия | |
| • образования | -3010,1 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | реагирует |
| Классификация | |
| Рег. номер CAS |
[1314-56-3] (P2O5) [16752-60-6] (P4O10) |
| Безопасность | |
| Предельная концентрация | 1 мг/м3 |
| ЛД50 | 100-140 мг/кг |
| Токсичность | Класс опасности 2 |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Пентаоксид фосфора, также оксид фосфора(V) (фосфорный ангидрид, пятиокись фосфора) — неорганическое химическое соединение класса кислотных оксидов с формулой P2O5. Белый кристаллический порошок, реагирует с водой; ядовит.
Строение
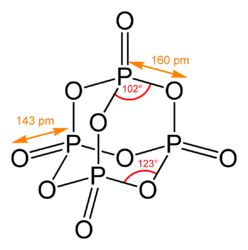
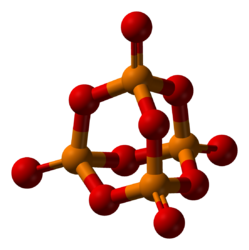
Пары оксида фосфора(V) имеют состав P2O5. Твёрдый оксид склонен к полиморфизму. Существует в аморфном стекловидном состоянии и кристаллическом. Для кристаллического состояния известны две метастабильные модификации пентаоксида фосфора — гексагональная Н-форма (а = 0,744 нм, = 87°, пространственная группа R3С) и орторомбическая О-форма (а = 0,923 нм, b = 0,718 нм, с = 0,494 нм, пространственная группа Рпат), а также одна стабильная орторомбическая О-форма (а =1,63 нм, b= 0,814 нм, с =0,526 нм, пространственная группа Fdd2). Молекулы P42O105 (Н-форма) построены из 4 групп PO4 в виде тетраэдра, вершины которого занимают атомы фосфора, 6 атомов кислорода располагаются вдоль рёбер, а 4 — по оси третьего порядка тетраэдра. Эта модификация легко возгоняется (360°С) и активно взаимодействует с водой.
Другие модификации имеют слоистую полимерную структуру из тетраэдров PO4, объединённые в 10-членные (О-форма) и 6-членные (О'-форма) кольца. Эти модификации имеют более высокую температуру возгонки (~580°С) и менее химически активны. H-форма переходит в О-форму при 300—360оC.
Свойства
P2O5 очень активно взаимодействует с водой при нагреве (H-форма поглощает воду даже со взрывом), образуя смеси метафосфорных кислот, состав которых зависит от количества воды и других условий:[math]\displaystyle{ \mathsf{P_2O_{5} + 3H_2O \rightarrow 2H_3PO_4} }[/math]
- При дальнейшем нагреве образует пирофосфорную кислоту:
- [math]\displaystyle{ \mathsf{2H_3PO_{4} \rightarrow H_4P_2O_7 + 2H_2O} }[/math]
- На холоде с водой образует метафосфорную кислоту:
- [math]\displaystyle{ \mathsf{P_2O_{5}+{H_2O} \rightarrow 2HPO_3} }[/math]
При сильном нагревании распадается на:
[math]\displaystyle{ \mathsf{P_2O_{5} \rightarrow P_4O_6 + 2O_2\uparrow} }[/math]
Он также способен извлекать воду из других соединений, представляя собой сильное дегидратирующее средство:
- [math]\displaystyle{ \mathsf{4HNO_3 + P_4O_{10} \rightarrow 4HPO_3 + 2N_2O_5} }[/math]
- [math]\displaystyle{ \mathsf{4HClO_4 + P_2O_{5} \rightarrow 4HPO_3 + 2Cl_2O_7} }[/math]
Оксид фосфора(V) широко применяется в органическом синтезе. Он реагирует с амидами, превращая их в нитрилы:
- [math]\displaystyle{ \mathsf{P_4O_{10} + RCONH_2 \rightarrow P_4O_9(OH_2) + RCN} }[/math]
Карбоновые кислоты переводит в соответствующие ангидриды:
- [math]\displaystyle{ \mathsf{P_2O_{5} + 12RCOOH \rightarrow 4H_3PO_4 + 6(RCO)_2O} }[/math]
Оксид фосфора(V) также взаимодействует со спиртами, эфирами, фенолами и другими органическими соединениями. При этом происходит разрыв связей P—О—P и образуются фосфорорганические соединения. Реагирует с NH3 и с галогеноводородами, образуя фосфаты аммония и оксигалогениды фосфора:
- [math]\displaystyle{ \mathsf{P_2O_{5} + 8PCl_3 + O_2 \rightarrow 12POCl_3} }[/math]
При сплавлении P4O10 с основными оксидами образует различные твёрдые фосфаты, природа которых зависит от условий реакции.
Оксид активно взаимодействует с водой, поэтому его часто используют в качестве осушителя.
Получение
Оксид фосфора(V) получают сжиганием фосфора в избытке кислорода или воздуха. Технологический процесс происходит в камере сжигания и включает в себя окисление элементарного P предварительно осушенным воздухом, осаждение P2O5 и очистку отходящих газов. Очищают полученный пентаоксид возгонкой.
- [math]\displaystyle{ \mathsf{4P + 5O_2 \rightarrow P_2O_{5}} }[/math]
Технический продукт имеет вид белой снегообразной массы, состоящей из смеси разных форм P4O10.
Основные сферы использования
P2O5 применяют как осушитель газов и жидкостей. Также он является промежуточным продуктом в производстве ортофосфорной кислоты H3PO4 термическим способом.
Широко используется в органическом синтезе в реакциях дегидратации и конденсации.
Физиологическое значение
Пентаоксид фосфора особо токсичен; относится ко второму классу опасности и в высоких концентрациях раздражает кожу и слизистые оболочки глаз.
ПДК в рабочей зоны - 1 мг/м³ (в соответствии с ГОСТ 12.1.005-76).
ЛД50 на крысах и белых мышах при пероральном введении составляет 140 мг/кг.
Литература
- Ахметов Н. С. «Общая и неорганическая химия» М.: Высшая школа, 2001
- Реми Г. «Курс неорганической химии» М.: Иностранная литература, 1963
- Ф. Коттон, Дж. Уилкинсон «Современная неорганическая химия» М.: Мир, 1969
- Зефиров Н.С. и др. т.5 Три-Ятр // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1998. — 783 с. — ISBN 5-85270-310-9.
- Кузьменко, Ерёмин, Попков Начала химии 1 том стр. 364
